(10分)在密闭容器中,使2 mol N2和6 mol H2混合发生下列反应:
N2(g)+3H2(g) 2NH3(g)(正反应为放热反应)
2NH3(g)(正反应为放热反应)
(1)当反应达到平衡时,N2和H2的浓度比是________;
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量________,密度________。(填“变大”“变小”或“不变”)
(3)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将________(填“向左移动”“向右移动”或“不移动”)。达到新平衡后,容器内温度________(填“大于”“小于”或“等于”)原来的2倍。
(共14分)Ⅰ.化学实验的微型化可有效地减少污染,实现化学实验绿色化的要求。某学生按下列操作做一个实验:在一块下衬白纸的玻璃片的不同位置分别滴加浓度为0.1 mol/L的KBr、KI(含淀粉溶液)、NaOH(含酚酞)、FeCl2(含KSCN)溶液各1滴,每种液滴彼此分开,围成半径小于表面皿的圆形(如下图所示),在圆心处放置2粒芝麻粒大小的KMnO4晶体,向KMnO4晶体滴加一滴浓盐酸,再立即用表面皿盖好。(已知2KMnO4+16HCl(浓)  2KCl +2MnCl2 +5Cl2↑+8H2O)
2KCl +2MnCl2 +5Cl2↑+8H2O)







 (1)e处反应的离子方程式为 。
(1)e处反应的离子方程式为 。
 该反应中氧化剂和还原剂的物质的量之比为 。
该反应中氧化剂和还原剂的物质的量之比为 。
 (2)b处的实验现象: 。
(2)b处的实验现象: 。
 d处的实验现象: 。
d处的实验现象: 。
 (3)c处反应的化学方程式为 。
(3)c处反应的化学方程式为 。

Ⅱ.混合物A由碳酸钠和碳酸氢钠组成。现有两包质量相等的混合物A:
(1)若向其中一包加入100mL 3mol/L的Ba(OH)2溶液(过量),使HCO3-、CO32-全部变为沉淀,过滤后,再向滤液中加入200mL 2mol/L的稀盐酸,溶液恰好呈中性。
①写出下列反应的离子方程式
碳酸氢钠与过量氢氧化钡的反应: ;
②混合物A中NaHCO3的质量为 g。 (2)若向另一包中先加50mL8mol/L的HCl溶液,使HCO3-、CO32-全部变为CO2后,再加50mL2mol/L的 Ba(OH)2溶液,混合后的溶液pH=14(混合后溶液体积变化忽略不计、在常温下)。混合物A中Na2CO3的质量为_______________g。
(2)若向另一包中先加50mL8mol/L的HCl溶液,使HCO3-、CO32-全部变为CO2后,再加50mL2mol/L的 Ba(OH)2溶液,混合后的溶液pH=14(混合后溶液体积变化忽略不计、在常温下)。混合物A中Na2CO3的质量为_______________g。
(共13分)由若干种可溶性物质组成的固体混合物X,可能含有的阳离子和阴离子分别是:


























| 阳离子 |
Na+Mg2+Al3+Ag+Ba2+ |
| 阴离子 |
OH-Cl- SO42- SO32-CO32- |

 为了鉴定其中的离子,现进行如下实验,试根据实验现象和要求填空。
为了鉴定其中的离子,现进行如下实验,试根据实验现象和要求填空。
 (1)取少许该白色固体加水溶解,最后得到无色溶液;用pH试纸检测,溶液的pH为13。则X中一定不存在的离子是_____________。
(1)取少许该白色固体加水溶解,最后得到无色溶液;用pH试纸检测,溶液的pH为13。则X中一定不存在的离子是_____________。
 (2)向溶液中滴加盐酸溶液,刚开始无沉淀,后有沉淀生成,继续滴加沉淀消失,并有无色无味气体逸出。则由(1)和(2)可得出的结论是:X中一定存在的离子有____________;又可确定X中一定不存在的离子有________________。
(2)向溶液中滴加盐酸溶液,刚开始无沉淀,后有沉淀生成,继续滴加沉淀消失,并有无色无味气体逸出。则由(1)和(2)可得出的结论是:X中一定存在的离子有____________;又可确定X中一定不存在的离子有________________。
 (3)若组成X的物质有三种,则可能是(用化学式表示,写出一组即可) ________________。
(3)若组成X的物质有三种,则可能是(用化学式表示,写出一组即可) ________________。
 (4)尚待检验的离子及检验方法是:
(4)尚待检验的离子及检验方法是:
| 尚待检验的离子 |
检验方法 |
            |
(共10分)A、B、C、D、E、F、G是中学里常遇到的一些物质,它们之间有如下转化关系,有些必要的信息已在框图中注明:
回答下列问题:
(1)D的空间构型为,C的电子式为,F溶液名称是,
(2)在实验室中制取气体A的离子方程式是.
(3)写出A+D→C的化学方程式 ,
氧化剂与还原剂物质的量之比为,
(4)写出:F+B(过量)→E的离子方程式 ,
(共7分)(1)在热的稀硫酸溶液中溶解了11.4gFeSO4.当加入50mL0.5mol/LKNO3
溶液后,使其中的Fe2+全部转化成Fe3+,KNO3也反应完全,并有NxOy氮氧化物气体逸出.
□FeSO4+□KNO3+□H2SO4→□K2SO4+□Fe2(SO4)3+□NXOy+□H2O
①推算出x=________,y=________.
②配平该化学方程式(系数填写在上式方框内)
③反应中氧化剂为________.
④用短线和箭头标出电子转移的方向和总数.
晶体具有规则的几何外形,晶体中最基本的重复单位称晶胞。氯化钠晶体结构如图所示,已知NixO晶体晶胞结构为氯化钠型,由于晶体缺陷,x值小于1,测知NixO晶体的密度为7.4g/cm3,晶胞边长为4.0×10-10m(NA用6.0x1023计算)。试回答(要求计算过程):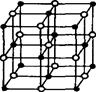
(1)NixO晶体中的x值_________(精确到0.01)。
(2)晶体中的Ni分别为Ni2+、Ni3+,此晶体化学式____________(用含Ni2+、Ni3+表示)。