(10分)某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g) FeO(s)+CO(g),测得CO2和CO浓度随时间的变化如图所示:
FeO(s)+CO(g),测得CO2和CO浓度随时间的变化如图所示: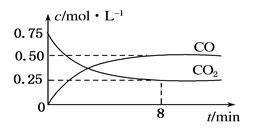
(1)0~8 min,v(CO)=______________________mol·L-1·min-1。
(2)下列措施中,能够改变平衡时c(CO)/c(CO2)的比值的是________(填选项字母)。
| A.温度 | B.铁粉的量(足量) | C.压强 | D.CO的量 |
(3)已知:反应Fe(s)+CO2(g) FeO(s)+CO(g)的平衡常数为K1;反应Fe(s)+H2O(g)
FeO(s)+CO(g)的平衡常数为K1;反应Fe(s)+H2O(g) FeO(s)+H2(g)的平衡常数为K2。不同温度时K1、K2的值如下表:
FeO(s)+H2(g)的平衡常数为K2。不同温度时K1、K2的值如下表:
| 温度/K |
K1 |
K2 |
| 973 |
1.47 |
2.38 |
| 1 173 |
2.15 |
1.67 |
根据表中数据,计算反应CO2(g)+H2(g)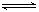 CO(g)+H2O(g)的K3
CO(g)+H2O(g)的K3
①温度为973 K时:K=_______________;
②温度为1 173 K时:K=________________;
③反应CO2(g)+H2(g)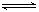 CO(g)+H2O(g)是________反应(填“吸热”或“放热”)。
CO(g)+H2O(g)是________反应(填“吸热”或“放热”)。
Ca(ClO)2与浓盐酸反应会生成Cl2,该反应的化学方程式为:
Ca(ClO)2 + 4HCl(浓)= CaCl2 + 2Cl2↑+ 2H2O
⑴浓盐酸在反应中显示出来的性质是(填写字母)
| A.只有还原性 | B.还原性和酸性 | C.只有氧化性 | D.氧化性和酸性 |
⑵产生0.3molCl2,则转移的电子的物质的量为
⑶该反应中氧化产物与还原产物的质量比为
⑷用双线桥法表示该氧化还原反应中电子转移的方向和数目
新制的氯水显色,说明氯水中有存在,蓝色石蕊试纸遇到氯水后,首先变红,起作用的成分是 ,但很快又褪色,起作用的成分是 ,氯水经光照后产生气体,该反应的化学方程式是
⑴用18mol/L浓硫酸配制100mL 1.0mol/L的稀硫酸,若实验仪器有:
A.100mL量筒 B.玻璃棒 C.托盘天平 D.50mL容量瓶
E.10mL量筒 F.胶头滴管 G.50mL烧杯 H.100mL容量瓶
实验时必须选用的仪器是(填入字母)
|
⑵在配制过程中,下列操作不正确的是
A.使用容量瓶前需检查它是否漏水CO与CO2的混合气体18g,在标准状况下体积为11.2 L,其中CO2的质量为__________,CO的物质的量为__________,则混合气体的平均摩尔质量为____________。
将1mol CO和1mol H2O充入某固定容积的反应器中,在某条件下达到平衡:CO+H2O(g)?CO2+H2,此时有2/3的CO转化为CO2。
(1)该平衡混合物中CO2的体积分数为__________。
(2)若在相同条件下,向容器中充入1mol CO2、1mol H2和1mol H2O,则达到平衡时与(1)中平衡相比较,平衡应向__________(填“正反应方向”、“逆反应方向”或“不”)移动,此时平衡混合物中CO2的体积分数可能是下列各值中的__________
| A.22.2% | B.27.55% | C.33.3% | D.36.8% |
(3)结合(2)中计算结果分析若平衡向正反应方向移动时,则下列说法中正确的是__________。
①生成物的产量一定增加;②生成物的体积分数一定增加;③反应物的转化率一定增大;④反应物的浓度一定降低;⑤正反应速率一定大于逆反应速率;⑥一定使用了催化剂