酸性溶液中,Fe2+会被空气缓慢氧化为Fe3+。不同条件下,一定浓度的Fe2+的氧化率随时间变化关系如下图所示。
下列有关说法正确的是
| A.该氧化过程的离子方程式为:Fe2++O2+4H+=Fe3++2H2O |
| B.其他条件相同时,80℃时Fe2+的氧化率比50℃的大 |
| C.Fe2+的氧化率仅与溶液的pH和温度有关 |
| D.pH=1.5时Fe2+的氧化率一定比pH=2.5的大 |
14CO2与碳在高温条件下发生反应:14CO2+C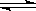 2CO,达到化学平衡后,平衡混合物中含14C的微粒有()
2CO,达到化学平衡后,平衡混合物中含14C的微粒有()
| A.14CO2 | B.14CO2、14CO | C.14CO2、14CO、14C | D.14CO |
已知NO2和N2O4可以相互转化:N2O4(g) 2NO2(g)△H <0。在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如下图。下列说法不正确的是
2NO2(g)△H <0。在恒温条件下将一定量NO2和N2O4的混合气体通入一容积为2 L的密闭容器中,反应物浓度随时间变化关系如下图。下列说法不正确的是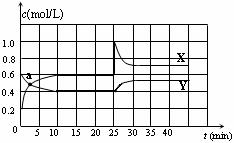
| A.图中的两条曲线,X是表示NO2浓度随时间的变化曲线 |
| B.a点时v(N2O4) = v(NO2) |
| C.25 min时改变了影响速率的一个因素,使得NO2转变为N2O4,该改变是将密闭容器的体积缩小,增大压强 |
| D.前10 min内用v(N2O4)表示的化学反应速率为0.02 mol/(L·min) |
下图所示的直型石英玻璃封管中充有CO气体,左端放置不纯的镍(Ni)粉。在一定条件下,Ni可以与CO(g)发生如下反应: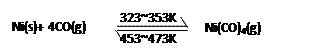

但Ni粉中的杂质不与CO(g)发生反应。玻璃管内左右两端的温度分别稳定在350K和470K,经过足够长时间后,下列说法正确的是
| A.在石英管右端主要物质是Ni(CO)4(g) |
| B.在石英管右端主要物质是纯Ni(s)和CO(g) |
| C.在石英管左端主要物质是纯Ni(s)和CO(g) |
| D.整个过程可以看作CO(g)将Ni(s)从石英管左端转移到右端,从而达到提纯目的 |
将V1mL1.0mol/L HCl溶液和V2mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如右图所示(实验中始终保持V1+V2=50mL)。下列叙述正确的是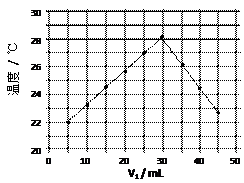
| A.做该实验时环境温度为22℃ |
| B.该实验表明化学能可能转化为热能 |
| C.NaOH溶液的浓度约为1.5mol/L |
| D.该实验表明有水生成的反应都是放热反应 |
右图是373K时N2与H2反应过程中能量变化的曲线图。下列叙述正确的是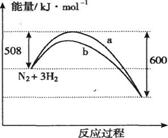
A.该反应的热化学方程式为:N2+3H2 2NH3△H=-92kJ·mol-1 2NH3△H=-92kJ·mol-1 |
| B.a曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,该化学反应的反应热不变 |
| D.在相同温度的条件下,在体积相同I、II两个容器中分别通入1mol N2和3 mol H2,容器I体积恒定,容器II体积可变保持恒压,则反应过程中两容器内的反应速率V(I)<V(II) |