X、Y、Z、R、W是原子序数依次增大的五种短周期元素。Y和R同主族,可组成共价化合物RY2和RY3,Y和Z最外层电子数之和与W的最外层电子数相同,25℃时0.0l mol/LX和W形成化合物的水溶液pH为2。下列说法不正确的是
| A.由于非金属性Y>R,则X、Y组成化合物的稳定性高于X、R组成的化合物 |
| B.在Z、Y形成的两种离子化台物中阴阳离子的个数比分别均为1:2 |
| C.原子半径由大到小排列的顺序是:Z>R>W>Y>X |
| D.Y、Z、W三种元素组成化合物的水溶液一定显碱性 |
在20g密度为dg/cm3的硝酸钙溶液里含1g Ca2+,则NO3-离子的物质的量浓度是
A.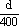 mol·L-1 mol·L-1 |
B.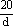 mol·L-1 mol·L-1 |
C.2.5d mol·L-1 | D.1.25 d mol·L-1 |
某原电池装置如图所示,电池总反应为2Ag+Cl2=2AgCl。下列说法正确的是
| A.正极反应为Cl2+2e-=2Cl- |
| B.放电时,交换膜右侧溶液中有大量白色沉淀生成 |
| C.若用NaCl溶液代替盐酸,则电池总反应随之改变 |
| D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.01 mol离子 |
Mg—H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,示意图如下。该电池工作时,下列说法正确的是
| A.Mg电极是该电池的正极 |
| B.H2O2在石墨电极上发生氧化反应 |
| C.石墨电极附近溶液的pH增大 |
| D.溶液中Cl-向正极移动 |
已知298K时,Mg(OH)2的溶度积常数为KSP=5.6×10-12,取适量的MgCl2溶液,加入一定量的烧碱溶液达到沉淀溶解平衡,测得pH=13.0,则下列说法不正确的是
| A.所得溶液中c(H+)=10-13 mol/L |
| B.所加烧碱溶液的pH=13.0 |
| C.所得溶液中由水电离产生的c(OH-)=10-13 mol/L |
| D.所得溶液中c(Mg2+)=5.6×10-10 mol/L |
溴酸银(AgBrO3)溶解度随温度变化曲线如图所示,下列说法错误的是
| A.溴酸银的溶解是吸热过程 |
| B.温度升高时溴酸银溶解速度加快 |
| C.60 ℃时溴酸银的Ksp约等于6×10-3 |
| D.若硝酸钾中含有少量溴酸银,可用它们的溶解度随温度变化的差异进行分离 |