根据以下三个热化学方程式:
2H2S(g)+3O2(g)===2SO2(g)+2H2O(l) ΔH=-Q1 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(l) ΔH=-Q2 kJ·mol-1
2H2S(g)+O2(g)===2S(s)+2H2O(g) ΔH=-Q3 kJ·mol-1
判断Q1、Q2、Q3三者关系正确的是 ( )
| A.Q1>Q2>Q3 | B.Q1>Q3>Q2 |
| C.Q3>Q2>Q1 | D.Q2>Q1>Q3 |
反应:Al2O3+N2+3C 2AlN+3CO,下列有关该反应叙述正确的是
2AlN+3CO,下列有关该反应叙述正确的是
| A.上述反应中,N2是还原剂,Al2O3是氧化剂 |
| B.AlN的摩尔质量为41 g |
| C.AlN中氮元素的化合价为+3 |
| D.上述反应中,每生成1 mol AlN需转移3 mol电子 |
下列有关说法正确的是
| A.焰色反应是化学变化 |
| B.CO2通入CaCl2溶液中会产生白色沉淀 |
| C.Fe3+遇KSCN溶液会产生红色沉淀 |
| D.25 ℃,Na2CO3在水中的溶解度比NaHCO3大 |
下列关于硅单质及其化合物的说法正确的是
①硅酸盐Na2Fe2Si3O10用氧化物的形式表示为:Na2O·2FeO·3SiO2
②水泥、玻璃、水晶饰物都是硅酸盐制品
③高纯度的硅单质广泛用于制作光导纤维
④单质硅是将太阳能转变为电能的常用材料
| A.②③ | B.①③ | C.①④ | D.④ |
下列离子方程式正确的是
| A.向NaHCO3溶液中加入少量的澄清石灰水:2HCO3-+Ca2++2OH-=CaCO3↓+CO32-+2H2O |
| B.FeCl3溶液与Cu的反应:Cu+ Fe3+="=" Cu2++ Fe2+ |
| C.醋酸溶液与水垢中的CaCO3反应:CaCO3+2 H+="=" Ca2++H2O+CO2↑ |
| D.氯化铝溶液中加入过量氨水:Al3++ 4 NH3•H2O ==AlO2- + 4 NH4+ + 2 H2O |
下列金属冶炼的反应原理,错误的是
A.2NaCl(熔融) 2Na+Cl2↑ 2Na+Cl2↑ |
B.MgO+H2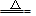 Mg+H2O Mg+H2O |
C.Fe3O4+4CO  3Fe+4CO2 3Fe+4CO2 |
D.2HgO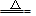 2Hg + O2↑ 2Hg + O2↑ |