在氯氧化法处理含CN-的废水过程中,液氯在碱性条件下可以将氰化物氧化成氰酸盐(其毒性仅为氰化物的千分之一),氰酸盐进一步被氧化为无毒物质。
(1)某厂废水中含KCN,其浓度为650mg / L。现用氯氧化法处理,发生如下反应(其中N均为-3价):KCN+2KOH+Cl2 → KOCN+2KCl+H2O 被氧化的元素是 。
(2)投入过量液氯,可将氰酸盐进一步氧化为氮气,请配平虾类方程式,并标出电子转移数目:
KOSN+ KOH+ Cl2→ CO2+ N2+ KCl+ H2O
(3)若处理尚书废水20L,使KCN完成转化为无毒物质,至少需要液氯 g。
【化学与技术】
从海水中提取一些重要的化工产品的工艺流程如图所示。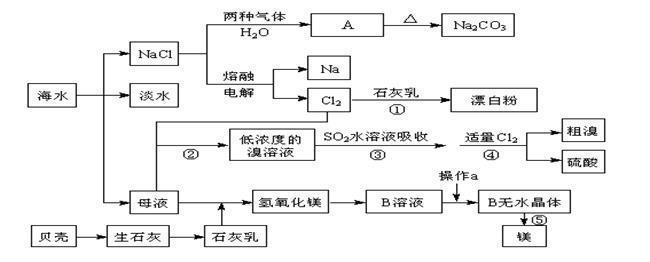
根据上述流程图回答下列问题:
(1)图中A的化学式为________________,在制取A的过程中需向饱和NaCl溶液中先后通入两种气体,后通入气体的化学式为_____________________。( 2分)
(2)海水淡化处理的方法有______________________________。(写出3种即可)( 3分)
(3)过程⑤的化学方程式为__________________________________________。( 2分)
(4)从B溶液制备B的无水晶体的“操作a”为_______________________________ 。( 2分)
(5)过程③用SO2水溶液吸收溴单质,吸收率可达93%,生成两种强酸,写出反应的离子方程式 _____________________________。( 2分)
(6)过程②到过程④的变化为“Br-→Br2→Br-→Br2”,其目的是____________。( 2分)
【离子推断】某混合溶液中,只可能大量含有下表所列离子中的某几种:
| 阳离子 |
H+、K+、Al3+、NH4+、Mg2+ |
| 阴离子 |
OH-、SO42-、CO32-、AlO2-、S2- |
将Na2O2逐渐加入到上述混合溶液中,产生沉淀的物质的量与加入Na2O2的物质的量的关系如图所示。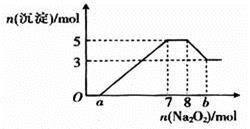
(1)将上述混合溶液中一定大量含有的阴、阳离子及其物质的量填入下表(可以不填满,也可以增加)。(每空1分)
| 离子种类 |
||||||
| 物质的量(mol) |
(2)图中a=____________, b=____________。
食用明胶是水溶性蛋白质混合物,具有很高的营养价值,溶于水形成胶体。而工业明胶中往往含有超标的重金属Cr,从而对人体造成伤害。
(1)已知Fe(CrO2)2中铬元素是+3价,则其中铁元素是___________价。
(2)化学上可将某些盐写成氧化物的形式,如Na2SiO3可写成Na2O·SiO2,则Fe(CrO2)2可写成________。
(3)明胶的水溶液和K2SO4溶液共同具备的性质是___________。
a.都不稳定,密封放置沉淀
b.两者均会发生丁达尔效应
c.分散质微粒可通过滤纸
(4)已知胶体的分散质微粒不能透过半透膜,但小分子或离子能透过半透膜。现将10 mL明胶的水溶液与5 mL NaBr溶液混合后装入半透膜袋内,将此半透膜袋浸入盛蒸馏水的烧杯中。若要求只检验一种离子, 就能证明Na+、Br-透过半透膜,写出检验该离子的实验方法:______________________
(5)铬的化合价除了+3和+6价外,还有0,+2,+4和+5价等。现有24 mL浓度为0.05 mol·L-1的Na2SO3溶液恰好与20 mL浓度为0.02 mol·L-1的Na2Cr2O7溶液完全反应,则元素Cr在还原产物中的化合价为____________价。
铁砂的主要成分是微粒状的磁性氧化铁、石英、石灰石的混合物。某化学兴趣小组从铁砂中分离出磁性氧化物,并进行铝热反应实验。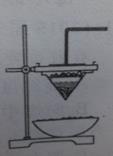
(1)取磁性氧化铁按图装置进行铝热反应,引发铝热反应的实验操作是_________________现象很壮观,取少许生成的“铁块”溶于盐酸,向其中滴加KSCN溶液,发现溶液变血红色。出现结果的原因,除了可能混有没有反应的磁性氧化铁外,还有一个原因是____________设计一个简单的实验方案,证明上述所得“铁块”中含有金属铝。该实验所用的试剂 是____________,反应的离子方程式_____________________
(2)写出此铝热反应的化学方程式:___________________________每摩尔单质铝参与反应,转移的电子数为___________________
(3)除磁性氧化铁可做铝热反应实验外,下列哪些试剂也可以()
| A.CuO | B.Na2O2 | C.MnO2 | D.MgO |
甲烷自热重整是先进的制氢方法, 包含甲烷氧化和蒸气重整。向反应系统同时通入甲烷、氧气和水蒸气, 发生的主要化学反应有:
回答下列问题:
(1)反应CO(g)+H2O(g)  CO2(g)+H2(g)的ΔH= kJ·mol-1。
CO2(g)+H2(g)的ΔH= kJ·mol-1。
(2)在初始阶段, 甲烷蒸气重整的反应速率 甲烷氧化的反应速率(填“大于”、“小于”或“等于”)。
(3)对于气相反应, 用某组分(B)的平衡压强(pB)代替物质的量浓度(cB)也可表示平衡常数(记作Kp), 则反应CH4(g)+H2O(g) CO(g)+3H2(g)的Kp= 随着温度的升高, 该平衡常数 (填“增大”、“减小”或“不变”)。
CO(g)+3H2(g)的Kp= 随着温度的升高, 该平衡常数 (填“增大”、“减小”或“不变”)。
(4)从能量角度分析, 甲烷自热重整方法的先进之处在于 。
(5)在某一给定进料比的情况下, 温度、压强对H2和CO物质的量分数的影响如下图: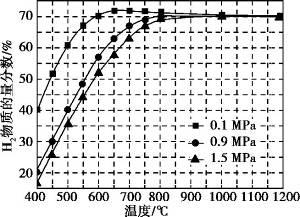
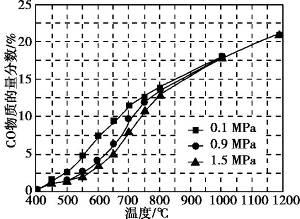
①若要达到H2物质的量分数>65%、CO物质的量分数<10%, 以下条件中最合适的是 。
A.600 ℃, 0.9 MPa B.700 ℃, 0.9 Mpa
C.800 ℃, 1.5 MPa D.1 000 ℃, 1.5 MPa
②画出600 ℃, 0.1 MPa条件下, 系统中H2物质的量分数随反应时间(从常温进料开始计时)的变化趋势示意图:
(6)如果进料中氧气量过大, 最终导致H2物质的量分数降低, 原因是 。