第五主族的磷单质及其化合物在工业上有广泛应用。
(1)同磷灰石在高温下制备黄磷的热化学方程式为:
4Ca5(PO4)3F(s)+21SiO2(s)+ 30C(s)=3P4(g)+20CaSiO3(s)+30CO(g)+SiF4(g) △H
已知相同条件下:
4Ca5(PO4)3F(s)+3SiO2(s)=6Ca3(PO4)2(s)+2CaSiO3(s)+SiF4(g) △H1
2Ca3(PO4)2(s)+10C(s)=P4(g)+6CaO(s)+10CO(g) △H2
SiO2(s)+CaO(s)=CaSiO3(s) △H3
用△H1、△H2和△H3表示△H , 则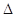 △H = ;
△H = ;
(2)白磷与氧气反应生成P4O10 固体。已知断裂下列化学键需要
吸收的能量分别为:
P—P a kJ·mol-1、 P—O b kJ·mol-1、
P==="O" c kJ·mol-1、 O==="O" d kJ·mol-1。
根据下图的分子结构和有关数据通过计算写出该反应的热化学方程式为 。
(3)三聚磷酸可视为三个磷酸分子(磷酸结构式如右图)之间脱去两个水分子产物,其结构式为_____________________,三聚磷酸钠(俗称“五钠”)是常用的水处理剂,其化学式为____________。
(4)次磷酸(H3PO2)为一元酸,分子中含一个羟基,其钠盐的正盐的化学式为 ,该盐可用于工业上的化学镀镍。
① 化学镀镍的溶液中含有Ni2+和H2PO2-, 在酸性等条件下发生下述反应:
(a)□Ni2+ + □H2PO2-+ □_____ = □Ni++ □H2PO3-+ □____
(b)6H2PO-2 + 2H+ =" 2P" + 4H2PO3 - + 3H2↑
请在答题卡上写出并配平反应式(a);
② 利用①中反应可在塑料镀件表面沉积镍—磷合金,从而达到化学镀镍的目的,这是一种常见的化学镀。请从以下方面比较化学镀与电镀。
原理上的不同点:______________________________________________________;
化学镀的优点:________________________________________________________。
A、B、C、D、E五种常见化合物,都是由下面中的离子形成的:阳离子:K+、Na+、Al3+、Fe3+,阴离子:HCO3-、SO42-、OH-、 Cl-
为了鉴别上述化合物,分别完成以下实验,其结果是:
① 将它们溶于水后,A为棕黄色溶液,其他均为无色溶液;
② 将它们进行焰色反应,仅有C、E为紫色(透过蓝色钴玻璃);
③ 将B溶液滴人到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
④ 在各溶液中加入硝酸钡溶液,再加过量稀硝酸,只有D中放出无色气体,只有A、C中产生白色沉淀;
⑤ 将A、E两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出化学式:A ____,C 。
(2)写出B和D反应的离子方程式: 。
(3)进行焰色反应实验操作时,使用铂丝前应该用 洗涤。
(4)在D溶液中加入少量澄清石灰水,其离子方程式为 。
(5)向100mL 1mol/L C溶液中加入0.2 mol Ba(OH)2溶液,充分反应后得到溶质是 。
利用化合价和物质类别推测物质的性质是化学研究的重要手段。
(1)从化合价的角度可以预测物质的性质。
①SO2中S元素处于中间价态,既有氧化性又有还原性;
②将SO2通入酸性KMnO4溶液中,溶液由紫红色褪至无色,SO2表现出 性质。
A.氧化性 B.还原性 C.既有氧化性又有还原性
(2)从物质分类的角度可以推测物质的性质。
①已知蛇纹石由MgO、Al2O3、SiO2、Fe2O3组成。其中SiO2属于 (填“酸性”、“碱性”或“两性”,下同)氧化物,Al2O3属于 氧化物。
②现取一份蛇纹石试样进行实验:
Ⅰ.先将其溶于过量的盐酸中,过滤,滤渣的主要成分是 ;
Ⅱ.再向滤液中加入NaOH溶液至过量,过滤,滤渣中的主要成分是 。
按要求填空:
(1)小苏打是某种治疗胃酸过多的胃药的主要成分,请写出该反应的离子方程式: 。
(2)金属钠在氧气中充分燃烧,将所得产物投入水中,产物和迅速发生反应,写出该反应的化学方程式: 。向所得溶液中加入FeSO4溶液,看到的现象是: ,此过程中发生的氧化还原反应的化学方程式: 。
(3)金属钙在一定条件下可以与氢气化合生成CaH2(白色固体)。将该白色固体加入滴有酚酞的蒸馏水中,可以观察到有气泡生成,溶液变红。请根据以上事实书写CaH2与水反应的化学方程式 。
下图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答问题: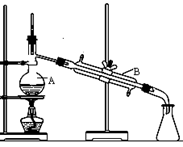

图1图2图3图4
(1)装置图1中A的名称是 。A 中一般要加入碎瓷片,其作用是 。若要从食盐溶液中得到食盐晶体,应选择的装置为 。
(2)为了从海带中提取碘,某研究性学习小组设计并进行了以下实验:
(已知苯是一种有机溶剂,密度比水小,不溶于水)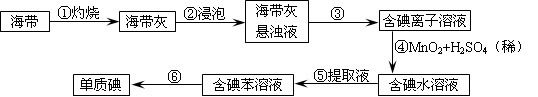
步骤③的实验选择上述装置图 (填图的序号)。步骤⑤的实验操作名称是 ,选择上述装置图 (填图的序号)。
将16.8g碳酸氢钠与11.7g过氧化钠固体混合后,在密闭容器中加热充分反应,排出气体物质后冷却,得到残余固体X。
(1)写出碳酸氢钠分解产生的气体分别与过氧化钠反应的化学反应方程式:
_________________、_________________________。
(2)残余固体X的成分是____________。
| A.Na2O2、NaOH | B.Na2O2、Na2CO3 | C.NaOH、Na2CO3 | D.Na2O2、NaOH、Na2CO3 |
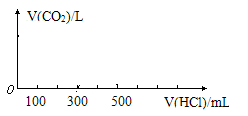
(3)向固体X中逐滴加入1mol/L的稀盐酸至不再产生气泡为止,产生的气体在标准状况下的体积为____L。请以V(HCl)为横坐标,V(CO2)为纵坐标,画出产生CO2的体积和加入稀盐酸溶液体积的关系。