化学反应可视为旧键断裂和新键形成的过程,化学键的键能是形成(或拆开)1mol 化学键时释放(或吸收)的能量。已知白磷和P4O6的分子结构如下图所示,现提供以下化学键的键能(KJ·mol–1)P–P:198 P–O:360 O=O:498 则反应P4(白磷,s)+ 3O2(g)==P4O6(s)的反应热△H为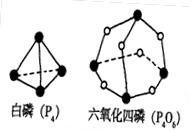
| A.+1638KJ·mol–1 | B.–1638KJ·mol–1 |
| C.+126KJ·mol–1 | D.–126KJ·mol–1 |
下列贮存化学试剂的方法正确的是
| A.在盛液溴的试剂瓶中加水,形成“水封”,以减少溴挥发 |
| B.用做感光片的溴化银贮存在无色试剂瓶中 |
| C.烧碱溶液放在带磨口玻璃塞的试剂瓶中 |
| D.新制的氯水保存在棕色广口瓶中,并放在阴凉处 |
设NA代表阿伏加德罗常数,下列说法正确的是
| A.22.4 L CO和CO2的混合气体中所含的碳原子数一定是NA |
| B.标准状况下,22.4 L氖气含有原子数为Na |
| C.物质的量浓度为2mol/L的BaCl2溶液中,含有Cl-个数为4NA |
| D.标准状况下,11.2L H2O含有0.5NA分子 |
下列溶液中溶质的物质的量浓度为1mol·L-1的是
| A.将40g NaOH溶解于1L水中配成的NaOH溶液 |
| B.将25g硫酸铜晶体溶于水制成100mL的溶液 |
| C.将1L 10mol/L的浓盐酸与9L水混合而成的溶液 |
| D.将100mL 1mol/L NaCl溶液加水稀释到200mL的溶液 |
amol H2中含有b个氢原子,则阿伏加德罗常数可以表示为
A. |
B.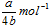 |
C.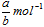 |
D.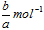 |
如图表示1 g O2与1 g X气体在恒压条件下的密闭容器中体积(V)与温度(T)的关系,则X气体可能是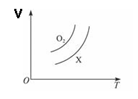
| A.C2H4 (气) | B.CH4 | C.CO2 | D.NO |