化学物I是治疗失眠症药物雷美替胺的中间体,其合成路线如下:
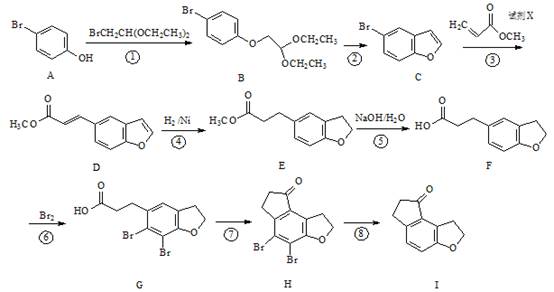
(1)反应④——⑧反应反应中,不属于取代反应的是 (填序号)。
(2)物质G中含氧官能团的名称为 、 。
(3)反应③中加入的试剂X的分子式为C4H6O2,X的结构简式为 。
(4)写出同时满足下列条件的物质I的一种同分异构体的结构简式 。
①能发生银镜反应;且水解产物之一能与FeCl3溶液发生显色反应。
②分子的核磁共振氢谱有5个峰,且分子中含有苯环。
(5)已知: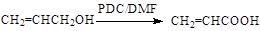
以 、
、 为原料,合成
为原料,合成 ,写出合成流程图(无机试剂任用)。合成流程图示例如下:
,写出合成流程图(无机试剂任用)。合成流程图示例如下:
二甲醚(CH3OCH3)是无色气体,可作为一种新型能源。由合成气(组成为H2、CO和少量的CO2)直接制备二甲醚,其中的主要过程包括以下四个反应:
甲醇合成反应:
(ⅰ)CO(g)+2H2(g)=CH3OH(g)ΔH 1 =-90.1kJ·mol-1
(ⅱ)CO2(g)+3H2(g)=CH3OH(g)+H2O(g) ΔH 2 =-49.0kJ·mol-1
水煤气变换反应:
(ⅲ)CO(g)+H2O(g)=CO2(g)+H2(g)ΔH 3=-41.1kJ·mol-1
二甲醚合成反应:
(ⅳ)2CH3OH(g)=CH3OCH3(g)+H2O(g)ΔH 4=-24.5kJ·mol-1
回答下列问题:
(1)Al2O3是合成气直接制备二甲醚反应催化剂的主要成分之一,工业上从铝土矿制备较高纯度Al2O3的主要工艺流程是(以化学方程式表示)。
(2)分析二甲醚合成反应(Ⅳ)对于CO转化率的影响。
(3)由H2和CO直接制备二甲醚(另一产物的水蒸气)的热化学方程式为。
根据化学反应原理,分析增加压强对直接制备二甲醚反应的影响。
(4)有研究者在催化剂(含Cu-Zn-Al-O和Al2O3)、压强为5.0MPa的条件下,由H2和CO直接制备二甲醚,结果如图所示。其中CO转化率随温度升高而降低的原因是。
下表为部分短周期主族元素的相关信息。
| 元素 |
相关信息 |
| T |
T的单质能与冷水剧烈反应,所得强碱性溶液中含有两种电子数相同的阴、阳离子 |
| X |
X的原子最外层电子数是其内层电子数的三倍 |
| Y |
在第三周期元素中,Y的简单离子半径最小 |
| Z |
T、X、Z组成的36电子的化合物A是家用消毒剂的主要成分 |
请回答下列问题:
(1)Z元素在元素周期表中的位置是第________周期第________族。
(2)元素T与X按原子个数比1∶1形成的化合物B所含的化学键有________(填化学键类型)。已知在通常状况下,39 g B与足量H2O反应放出Q kJ的热量,写出该反应的热化学方程式:__________________。
(3)将T的最高价氧化物对应水化物的溶液,逐滴加入到Y与Z形成的化合物的水溶液中,直至过量(边滴加边振荡),此过程中的现象是________________________。
(4)已知1 mol化合物A与足量Na2SO3在溶液中发生反应时,转移2 mol电子,写出该反应的离子方程式:_______________________________________。
如图所示,一密闭容器被无摩擦、可滑动的两隔板a、b分成甲、乙两室;标准状况下,在乙室中充入0.6mol HCl,甲室中充入NH3、H2的混合气体,静止时活塞位置如下图。已知甲、乙两室中气体的质量之差为10.9g。
(1)甲室中气体的物质的量为。
(2)甲室中气体的质量为。
(3)甲室中NH3,H2的物质的量之比为。
(4)将隔板a去掉,发生下列反应:HCl(g)+NH3(g)=NH4Cl(s),当HCl与NH3充分反应后,活塞b将位于刻度“”处(填数字)。
【化学——选修5:有机化学基础】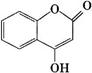 可用来制备抗凝血药,通过下列路线合成:
可用来制备抗凝血药,通过下列路线合成:
(1)A与银氨溶液反应有银镜生成,写出该反应的离子方程式 ;。
(2)B→C的反应类型是______________________________________。
(3) 写出D→E的化学方程式: _____________________________________。
(4)写出F和过量NaOH溶液共热时反应的化学方程式: _______________________________________。
(5)下列关于G的说法正确的是_____。
| A.能与溴单质反应 | B.能与金属钠反应 |
| C.1 mol G最多能和3 mol氢气反应 | D.分子式是C9H6O3 |
(6)E的同分异构体很多,除E外符合下列条件的共种。
①含苯环且能与氯化铁溶液显色, ②苯环上有两个取代基, ③含酯基。
(7)F分子中有种不同化学环境的氢原子
【化学——选修物质结构与性质】X、Y、Z、M、N、Q 、P为元素周期表前四周期的7种元素。其中,X原子核外的M层中只有两对成对电子,Y原子核外的L层电子数是K层的两倍,Z是地壳内含量最高的元素,M的内层电子数是最外层电子数的9倍,N的原子序数比M小1, Q在元素周期表的各元素中电负性最大。P元素的第三电子层处于全充满状态,第四电子层只有一个电子请回答下列问题:
(1)X元素在周期表中的位置是,它的外围电子的电子排布图为。P元素属于区元素,
(2)XZ2分子的空间构型是,YZ2分子中Y的杂化轨道类型为,相同条件下两者在水中的溶解度较大的是(写分子式),理由是 ____________________。
(3)含有元素N的盐的焰色反应为色,许多金属盐都可以发生焰色反应,其原因是
(4)元素M与元素Q形成晶体结构如图所示,设其晶胞边长为a pm,该化合物的摩尔质量为Dg/mol。
求该晶胞密度的计算式为g/cm3
(5)三聚氰胺是一种含氮化合物,其结构简式如图2所示。
三聚氰胺分子中氮原子轨道杂化类型是 ,
1 mol三聚氰胺分子中 σ键的数目为 。