请结合化学反应原理回答下列问题:
(1)硫酸的产量通常用来衡量一个国家的化学工业发展水平,硫酸工业生产中涉及反应之一为:
2SO2(g)+O2(g) 2SO3(g),SO2的平衡转化率与温度、压强的关系如右图所示。
2SO3(g),SO2的平衡转化率与温度、压强的关系如右图所示。
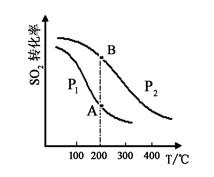
①压强:P1 P2(填“>”、“=”或“<”)。
②200℃下,将一定量的SO2和O2充入体积不变的密闭容器中,经10min后测得容器中各物质的物质的量浓度如下表所示:
| 气体 |
SO2 |
O2 |
SO3 |
| 浓度(mol/L) |
0.4 |
1.2 |
1.6 |
能说明该反应达到化学平衡状态的是 。
a.反应速率υ(SO2)=υ(SO3)
b.体系的压强保持不变
c.混合气体的密度保持不变
d.SO2和O2的体积比保持不变
计算上述反应在0~10min内,υ(SO2)= 。
(2)SO2与氢氧化钠溶液反应可以生成亚硫酸氢钠,已知25℃时,NaHSO3的水解平衡常数=1.0×10-12mol/L,则该温度下H2SO3 HSO3-+H+的电离常数Ka=____mol/L,若向H2SO3溶液中加入少量的I2,则溶液中
HSO3-+H+的电离常数Ka=____mol/L,若向H2SO3溶液中加入少量的I2,则溶液中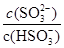 将________(填“增大”、“减小”或“不变”)。
将________(填“增大”、“减小”或“不变”)。
(3)工业制取硫酸还可以利用电化学原理:
①工业生产中用SO2为原料制取硫酸可以利用原电池原理,用SO2、O2和H2O来制备硫酸,该电池用多孔材料作电极,它能吸附气体,同时也能使气体与电解质溶液充分接触。请写出该电池的正极电极反应式_____________。
②用Na2SO3溶液充分吸收SO2得NaHSO3溶液,然后电解该溶液可制得硫酸。电解原理示意图如下图所示。请写出开始时阳极反应的电极反应式_________。

硝酸铵是含氮量较高的化肥,生产流程如下(产物水均已略去):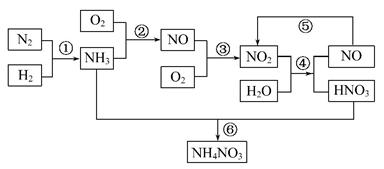
(1)反应④的化学方程式为3NO2+H2O====2HNO3+NO,该反应的氧化剂为 ,还原剂为 。
(2)补充并配平反应②的化学方程式:
NH3+ O2 NO+ 。
NO+ 。
(3)化学反应 (填序号)是非氧化还原反应,离子方程式为 。
(4)有人设计了一个反应来制备硝酸:NO2+NH3 HNO3+H2O(未配平),你认为该反应
HNO3+H2O(未配平),你认为该反应
(填“能”或“不能”)发生,理由是 。
A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):
A B
B C
C D。
D。
(1)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使湿润的蓝色石蕊试纸变红,则A为 。写出A→B转化的化学方程式:
。
(2)若A为活泼金属元素的单质,D为强碱,焰色反应显黄色,则C是 。A跟水发生反应的离子方程式为 。
)氮元素的化合价较多,负价态氮与正价态氮之间发生氧化还原反应时会有氮气产生。下面是甲、乙两位学生提出的两种制备少量氮气的实验方案(箭头表示气体的流向)。
甲:空气→碱石灰→红磷(点燃)→水→铜粉(灼热)→集气瓶
乙:NH4NO2(加热)→浓硫酸→镁粉(灼热)→集气瓶(提示:NH4NO2 N2↑+2H2O)
N2↑+2H2O)
回答下列问题:
(1)甲、乙两位学生的实验方案是否能制氮气?
甲 、乙 (填“能”或“不能”)。
(2)具体说明不能制取氮气的原因并纠正(若两种方案都能制氮气,此小题不用回答) 。
(3)甲方案中碱石灰和乙方案中浓硫酸可否交换位置?说明理由:
。
今年我国多个城市遭雾霾天气,这表明污染严重,空气质量下降。因此研究NO2、SO2、CO等大气污染气体的处理具有重要现实意义。
(1)NO2可用水吸收,相应的化学反应方程式为 。
(2)利用反应6NO2+8NH3 7N2+12H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是 L。
7N2+12H2O也可处理NO2。当转移1.2 mol电子时,消耗的NO2在标准状况下是 L。
(3)硝酸工业尾气中含NO和NO2气体,常用NaOH溶液来吸收,反应方程式为NO+NO2+2NaOH====2NaNO2+H2O,该反应中氧化剂和还原剂的物质的量之比是 。
(4)SO2是形成酸雨的主要物质,可以用氨水吸收消除污染,写出过量氨水与SO2反应的离子方程式 。
含硫化合物的种类很多,现有H2SO4、H2SO3、SO2、Na2SO3、BaSO4、CuSO4、Na2SO4这7种常见的含硫化合物。回答下列问题:
(1)H2SO3转化为硫酸是酸雨形成的重要过程之一,写出其反应的化学方程式,并标明电子转移方向和数目
。
(2)Ba2+有剧毒。某市曾发生一起“毒烧饼”事件,起因是烧饼摊主在制作烧饼的过程中误将碳酸钡当作干粉使用,导致多人食用烧饼后中毒。试写出碳酸钡与胃酸(以盐酸表示)反应的离子方程式
。
患者被送往医院后,医生往往让其服用
(填题干所列7种物质中的1种)来解毒。
(3)常温下,将铁棒置于浓硫酸中,无明显现象,有人认为未发生反应。为验证此过程,某同学经过思考,设计了如下实验:将经浓硫酸处理过的铁棒洗净后置于CuSO4溶液中,若铁棒表面
,
则发生了钝化;若铁棒表面 ,则未发生反应。