某火力发电厂以煤为燃料,充分燃烧后将热能转化为电能,其排出的废气中含有CO2、SO2、水蒸气等。为了检验该发电厂排出的废气中的成分,用如图所示的装置进行实验:
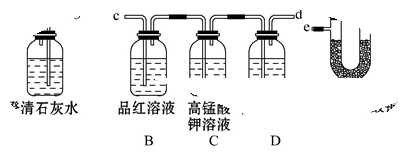
(1)仪器连接的顺序为(填导管接口字母) 。
(2)根据 现象能证明有SO2存在。
(3)根据 中无明显变化和装置A中 现象证明有CO2存在。
(4)把装置E放置在最后,能否证明该废气中含有水蒸气? ,理由是 。
(5)装置B的作用是 ,装置D的作用是 。
(6)将SO2通入氯水中溶液颜色变浅原因是___________________。
(1)五种元素的原子电子层结构如下:A:1s22s22p63s2 B:1s22s22p63s23p63d54s2 C:1s22s1 D:1s22s22p63s23p2 E:1s22s22p6。请回答:(填元素符号)
元素的电负性最大, 元素原子的第一电离能最小, 元素最可能生成具有催化性质的氧化物。
(2)钛和钛的合金已被广泛用于制造电讯器材、人造骨骼、化工设备、飞机等航天航空材料,被誉为“未来世界的金属”,钛有4822Ti和5022Ti两种原子,它们互称为 。Ti元素在元素周期表中的位置是第 ,按电子排布Ti元素在元素周期表分区中属于 区元素。
(3)A、B两种元素的电离能数据如下(kJ·mol—1):
| 电离能/kJ•mol-1 |
I1 |
I2 |
I3 |
I4 |
| A |
577 |
1817 |
2745 |
11578 |
| B |
738 |
1451 |
7733 |
10540 |
化合价是元素的一种性质。由A、B的电离能数据判断,A通常显价,B显 价。
(4)气态氯化铝(Al2Cl6)是具有配位键的化合物,分子中原子间成键的关系如下图所示。请将图中你认为是配位键的斜线上加上箭头。
(5)假设原子晶体SiO2中Si原子被铝原子取代,不足的价数由钾原子补充。当有25%的硅原子被铝原子取代时,可形成正长石。则正长石的化学组成为。
(6)CO2与SiO2比较沸点相差很大的原因是。
(1)某学生欲用铁片与2mol·L-1盐酸反应来制取少量氢气,现欲提高化学反应速率,实验中可采用①;②;③_________等方法;(2)碳酸钠溶液与盐酸的反应若欲降低化学反应速率可采取的方法有①;②________________________。
下列3种有机化合物A:CH2=CH2、 B: 、 C:CH3COOH
、 C:CH3COOH
(1)写出化合物A、C中的官能团、。
(2)能使溴的四氯化碳溶液褪色反应的化学方程式为:,
该反应类型为:。
(3)能与乙醇发生酯化反应的化学方程式为:,
(4) 在浓硫酸作用下,与浓硝酸反应的反应类型为:。
在浓硫酸作用下,与浓硝酸反应的反应类型为:。
下表是元素周期表中短周期元素部分,表中字母分别代表一种元素:
| a |
b |
||||||
| d |
e |
f |
|||||
| c |
g |
h |
(1)上述 元素(填元素名称)可以形成硬度最大的单质。
(2)“神舟”六号飞船内需要有一种化合物来吸收宇航员呼出的 CO2,并释放出O2,你认为该
物质应该是由上表中的 和 元素(填元素名称)组成的。飞船中需要制造一种适合宇航员生存的人工生态环境,应该在氧气中充入一种气体用于稀释氧气,该气体分子是 。
(3)表中元素g的氢化物稳定性比元素e的氢化物的稳定性 (填“强”或“弱”)。
(4)将潮湿的由h元素构成的单质通过甲装置后,再通过放有干燥红色布条的乙装置,红色布条不褪色。则甲装置中所盛试剂可能是
|
①浓硫酸②NaOH溶液③KI溶液④饱和食盐水
(5)写出h元素构成的单质与水反应的化学方程式: 。在原子序数1—18号元素中,按要求用合适的化学用语填空:
(1)与水反应最剧烈的金属是_____________。
(2)与水反应最剧烈的非金属单质是_____________。
(3)原子半径最小的元素是______________。
(4)最稳定气态氢化物的化学式是______________。
(5)最高价氧化物对应水化物的酸性最强的化学式是_______________。
(6)电子数为10的化合物分子式__、__、__、__。