现有一瓶物质甲和乙的混合物,已知甲和乙的某些性质如下:
| 物质 |
分子式 |
熔点/℃ |
沸点/℃ |
密度/(g/cm3) |
水中溶解性 |
| 甲 |
C3H6O2 |
-98 |
57.5 |
0.93 |
可溶 |
| 乙 |
C4H8O2 |
-84 |
77 |
0.90 |
可溶 |
据此,将甲和乙互相分离的最佳方法是( )
A.萃取法 B.升华法 C.蒸馏法 D.分液法
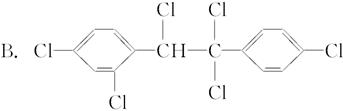
六氯苯是被联合国有关公约禁止或限制使用的有毒物质之一。下式中能表示六氯苯的是( )


CaC2、MgC2、Al4C3都是离子化合物,下列叙述不正确的是( )
| A.MgC2、Al4C3都能跟水反应生成乙炔 |
B. 的电子式为 的电子式为 |
| C.它们与水的反应属于水解反应 |
| D.Al4C3与水反应可得到甲烷 |
下列实验能获得成功的是( )
| A.乙醇与4 mol·L-1的硫酸混合加热到170 ℃制乙烯 |
| B.苯与浓溴水反应制取溴苯 |
| C.重油在常压下分馏可得石蜡、润滑油等 |
| D.电石与饱和食盐水作用制乙炔 |
据报道,近来发现了一种新的星际分子氰基辛炔,其结构式为:HC≡C—C≡C—C≡C—C≡N。对该物质判断正确的是( )
| A.晶体的硬度与金刚石相当 |
| B.能使高锰酸钾酸性溶液褪色 |
| C.不能发生加成反应 |
| D.可由乙炔和含氮化合物加聚制得 |
烯烃在一定条件下发生氧化反应时,C==C双键发生断裂。RCH="=CHR′" 可以被氧化成RCHO和R′CHO,在该条件下,下列烯烃分别被氧化后,产物中可能有CH3CHO的是( )
| A.(CH3)2C==CH(CH2)2CH3 |
| B.CH2==CH(CH2)2CH3 |
| C.CH3CH==CH—CH==CHCH3 |
| D.CH3CH2CH==CHCH2CH3 |