已知1.505×1023个X气体分子的质量为8g,则X气体的摩尔质量是
| A.16g | B.32g | C.64g /mol | D.32g /mol |
设NA为阿伏伽德罗常数的值。下列说法正确的是
A.5NH4NO3 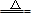 2HNO3+4N2↑+9H2O反应中,生成28 g N2,转移的电子数目为3.75NA 2HNO3+4N2↑+9H2O反应中,生成28 g N2,转移的电子数目为3.75NA |
| B.室温下,1 L pH=13的NaOH溶液中,由水电离的OH- 数目为0.1NA |
| C.氢氧燃料电池正极消耗22.4 L(标准状况)气体时,电路中通过的电子数目为2NA |
| D.高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3 NA |
常温下,下列各组离子在指定溶液中一定能大量共存的是
| A.能使酚酞变红的溶液:Na+、Ba2+、NO3-、Cl- |
| B.含有0.1 mol·L-1 Fe3+的溶液中:K+、Mg2+、I-、SO42- |
| C.能溶解Al(OH)3的溶液:NH4+、K+、SO42-、HCO3- |
| D.c(Al3+)="0.5" mol·L-1的溶液中:Na+、K+、AlO2-、SO42- |
化学在生产和日常生活中有着重要的应用。下列说法不正确的是
| A.华裔科学家高琨在光纤传输信息领域中取得突破性成就,光纤的主要成分是高纯度的二氧化硅 |
| B.工业上用石灰对煤燃烧后形成的烟气进行脱硫,并能回收得到石膏 |
| C.“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”都能提高空气质量 |
| D.电解MgCl2溶液,可制得金属镁 |
下列图像与所对应的叙述正确的是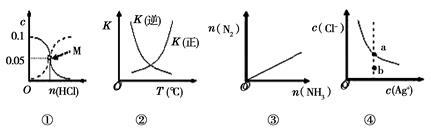
| A.图①表示室温下,用0.1 mol•L-1的氨水吸收HCl气体时,溶液中的粒子浓度随HCl体积的变化。实现表示c(NH3·H2O),虚线表示c(NH4+),处于M点时溶液呈中性 |
B.图②表示2SO2(g)+O2(g)  2SO3(g)△H<0,正逆反应的平衡常数随温度的变化 2SO3(g)△H<0,正逆反应的平衡常数随温度的变化 |
C.图③表示2NH3(g) N2(g) +3H2(g),在恒温恒压的密闭容器中达平衡时N2的物质的量随的 NH3物质的量的变化 N2(g) +3H2(g),在恒温恒压的密闭容器中达平衡时N2的物质的量随的 NH3物质的量的变化 |
D.图④表示AgCl(s) Ag+(aq) +Cl-(aq)的离子浓度关系,当处于b点时,蒸发部分水后,可到达平衡线的a点 Ag+(aq) +Cl-(aq)的离子浓度关系,当处于b点时,蒸发部分水后,可到达平衡线的a点 |
铅酸蓄电池是目前应用普遍的化学电池,新型液流式铅酸蓄电池以可溶性的甲基磺酸铅为电解质,电池总反应为:Pb+PbO2+4H+ 2Pb2++2H2O。下列有关新型液流式铅酸蓄电池的说法正确的是
2Pb2++2H2O。下列有关新型液流式铅酸蓄电池的说法正确的是
| A.放电时负极反应式为Pb-2e﹣+SO42﹣=PbSO4 |
| B.充放电时,溶液的导电能力变化不大 |
| C.以该电池电解NaCl溶液时,当消耗207gPb时,在阳极生成Cl222.4L |
| D.充电时的阳极反应式为Pb 2++2e-+4OH﹣=PbO2+2H2O |