铁是人类较早使用的金属之一。运用铁及其化合物的有关知识,回答下列问题:
(1)铁和铁合金是生活中的常用材料,下列叙述中,正确的是
A.纯铁硬度比生铁高
B.纯铁耐腐蚀性强,不易生锈
C.不锈钢是铁合金,只含金属元素
D.铁在一定条件下,可与水蒸气反应
E.铁在冷的浓硫酸中钝化
(2)向沸水中逐滴滴加1mol·L-1FeC13溶液,至液体呈透明的红褐色,该反应的离子方程式为 ,形成该分散系的微粒粒度范围是 。
(3)电子工业需用30%的FeC13溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。请写出 FeC13溶液与铜反应的离子方程式 。欲从腐蚀后的废液中回收铜并重新获得FeC13溶液,现有下列试剂:①氯气②铁粉③浓硝酸④浓盐酸⑤烧碱⑥浓氨水,需要用到的一组试剂是
A.①②④ B.①③④⑥ C.②④⑤ D.①④⑥
(4)高铁酸钠Na2FeO4是一种新型净水剂。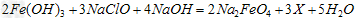 ①高铁酸钠主要通过如下反应制取:
①高铁酸钠主要通过如下反应制取:
则X的化学式为_______ ______。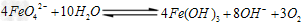 ②高铁酸钠在水中可以发生如下反应:
②高铁酸钠在水中可以发生如下反应:
由此看来,高铁酸钠能够杀菌消毒是因为它具有________性,而能够除去水中悬浮物是因为__________。
③ 下列物质能作净水剂的有 。
A.KAl(SO4)2·12H2O B.[Fe(OH)(SO4)]n C.ClO2 D.“84”消毒液
欲降低废水中重金属元素铬的毒性,可将Cr2O 转化为Cr(OH)3沉淀除去。三种金属离子生成沉淀的pH如下表。
转化为Cr(OH)3沉淀除去。三种金属离子生成沉淀的pH如下表。
| 开始沉淀的pH |
完全沉淀的pH |
|
| Fe(OH)2 |
7.0 |
9.0 |
| Fe(OH)3 |
1.9 |
3.2 |
| Cr(OH)3 |
6.0 |
8.0 |
某含铬废水处理的主要流程如下图所示: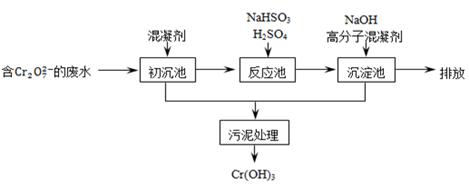
(1)Cr在周期表中的位置为。
(2)初沉池中加入明矾作沉降剂,其作用的原理是(用离子方程式表示)。
(3)请补充并配平以下反应池中发生主要反应的离子方程式:
____Cr2O72-+ ____HSO3-+ _______ = ____Cr3+ + ___SO42-+ ____H2O。
(4)根据“沉淀法”和“中和法”的原理,向沉淀池中加入NaOH溶液,此过程中发生主要反应的离子方程式是:H++OH- = H2O和____________________。证明Cr3+沉淀完全的方法是______________________。
现有七种元素,其中A、B、C、D、E为短周期主族元素,F、G为第四周期元素,它们的原子序数依次增大。A元素的核外电子数和电子层数相等,B元素原子的核外p电子数比s电子数少1, C原子的第一至第四电离能:I1=738 kJ·mol-1、I2=1451 kJ·mol-1、I3=7733 kJ·mol-1、I4=10540 kJ·mol-1,D原子价电子层的p轨道半满,E元素的主族序数与周期数的差为4, F是前四周期中电负性最小的元素,G在周期表的第七列。
(1)BA3的电子式为________,晶体类型为。
(2)B元素基态原子中能量最高的电子,其电子云在空间有________个取向,原子轨道呈________形。
(3)某同学根据上述信息,推断C基态原子的核外电子排布图为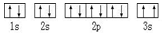 ,该同学所画的电子排布图违背了__________________。
,该同学所画的电子排布图违背了__________________。
(4)比较B和D的电负性较大的是________(填元素符号),BE3中心原子的杂化类型,其分子构型为。
(5)G位于周期表的________区,该元素的核外电子排布式为。
(6)检验F元素的方法是____________。
(1)X、Y、Z三种元素的离子结构都和Ar具有相同的电子层排布.H2在X单质中燃烧,产生苍白色火焰;Y元素的气态氢化物是H2Y,其最高价氧化物中Y的质量分数为40%;Z元素和氮元素在同一族.
①根据以上条件,推断X,Y,Z(填写元素符号);
②写出它们的最高价氧化物的水化物的化学式:X,Y,Z.
③写出Y在周期表中的位置_____________.
(2)下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,用化学用语回答下列问题。
a.④、⑤、⑥的原子半径由大到小的顺序是___________。
b.②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是___________。
c.③、④、⑥元素可形成含10个电子的微粒,其中A和B为分子,C和E为阳离子,D为阴离子;B溶于A后所得的物质可电离出C和D;A、B、E三种微粒反应后可得C和一种白色沉淀。用化学式表示下列4种微粒A ___________、B___________、C___________、D ___________并写出A、B、E三种微粒反应的离子方程式___________。
d.②和浓硫酸反应的化学方程式为___________
硫酸的性质有:
| A.强酸性; | B.吸水性; | C.脱水性; | D.强氧化性。 |
在下列硫酸的用途或化学反应中,硫酸可能表现上述的一个或者多个性质,试用字母填空:
(1)实验室干燥氢气___________________;
(2)浓硫酸与金属铜的反应________________;
(3)实际生产中,浓硫酸可用钢瓶贮运_________;
(4)浓硫酸使蔗糖变黑,且有刺激性气味的气体产生_______________。
为了测定某有机物A的结构,做如下实验;
①将4.6 g该有机物完全燃烧,生成0.2mol CO2和5.4g水;
②用质谱仪测定其相对分子质量,得如下图一所示的质谱图;
③用核磁共振仪处理该化合物,得到如图二所示谱图,图中三个峰的面积之比是1:2:3.
试回答下列问题:
(1)有机物A的相对分子质量是__________.
(2)有机物A的结构简式是__________.
(3) 写出有机物A的同分异构体的结构简式_______________.
(4) 写出由有机物A制备1,2-二氯乙烷过程的方程式