下列措施不合理的是( )
| A.用SO2漂白纸浆和草帽辫 |
| B.用硫酸清洗锅炉中的水垢 |
| C.高温下用焦炭还原SiO2制取粗硅 |
| D.用Na2S做沉淀剂,除去废水中的Cu2+和Hg2+ |
化学反应前后肯定没有变化的是()
①原子数目 ②分子数目 ③元素种类 ④物质的总质量 ⑤物质的种类
| A.①③④ | B.①③⑤ | C.③④⑤ | D.①②③④ |
某溶液中含有Ag+、Ba2+、Mg2+离子,为了将这三种离子逐个沉淀分离,加入下列离子的先后顺序正确的是()
| A.CO32-、 Cl-、OH- |
| B.Cl-、CO32-、OH- |
| C.OH-、Cl-、 CO32- |
| D.Cl-、OH-、CO32- |
在甲、乙两烧杯溶液中,分别含有大量的Cu2+、K+、H+、 Cl-、CO32-、OH-6种离子中的3种,已知甲烧杯的溶液呈蓝色,则乙烧杯的溶液中大量存在的离子是( )
| A.Cu2+、H+、Cl- |
| B.CO32-、OH-、Cl- |
| C.K+、H+、Cl- |
| D.K+、OH-、CO32- |
下列各组离子中,能在强酸溶液里大量共存,并且溶液呈无色透明的是()
A.MnO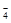 ,K+,Na+,SO ,K+,Na+,SO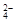 |
B.Na+,K+,HCO ,Cl- ,Cl- |
C.Mg2+,NH ,Cl-,NO ,Cl-,NO |
D.Ba2+,K+,S2-,SO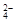 |
能用H+ + OH- = H2O表示的是()
| A.Ba(OH)2溶液和稀H2SO4的反应 |
| B.Cu(OH)2和稀H2SO4的反应 |
| C.NaOH溶液和氢溴酸反应 |
| D.NaOH溶液和醋酸溶液的反应 |