在密闭容器中发生如下反应:mA(g) + nB(g)  pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法错误的是
pC(g),达到平衡后,保持温度不变,将气体体积缩小到原来的一半,当达到新平衡时,C的浓度为原来1.9倍,下列说法错误的是
| A.m+n>p | B.平衡向逆反应方向移动 |
| C.A的转化率降低 | D.C的体积分数减小 |
下列离子方程式正确的是 ()
| A.向盐酸中滴加氨水:H+ + OH- = H2O |
| B.Fe(OH)3溶于氢碘酸:Fe(OH)3 + 3H+ = Fe3+ + 3H2O |
| C.铜溶于稀硝酸:3Cu + 8H+ + 2NO3- = 3Cu2+ + 2 NO ↑+ 4H2O |
| D.向Na2S2O3溶液中通入足量氯气:S2O32-+2Cl2+3H2O=2SO32-+4Cl-+6H+ |
有一瓶Na2SO3溶液,由于它可能部分被氧化,某同学进行如下实验:取少量溶液,滴入Ba(NO3)2溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,仍有白色沉淀。对此实验下述结论正确的是()
| A.Na2SO3已部分被空气中的氧气氧化 |
| B.加入Ba(NO3)2溶液后,生成的沉淀中一定含有BaSO4 |
| C.此实验不能确定Na2SO3是否部分被氧化 |
| D.加硝酸后的不溶沉淀一定是BaSO3 |
为贮存、运输、使用的方便,工业上常将H2O2转化为固态的过碳酸钠晶体(其化学式为2Na2CO3?3H2O2),该晶体具有Na2CO3和H2O2的双重性质。下列物质不会使过碳酸钠晶体较快失效的是()
| A.MnO2 | B.H2S | C.稀硫酸 | D.NaHCO3 |
将17.9gAl、Fe、Cu组成的合金溶于足量的NaOH溶液中,产生气体3.36L(标准状况)。另取等质量的合金溶于过量的稀硝酸中,生成6.72L NO(标准状况,唯一还原产物),向反应后的溶液中加入过量的NaOH溶液,得到沉淀的质量为( )
)
| A.33.2g | B.25.4g | C.22.4g | D.19.6g |
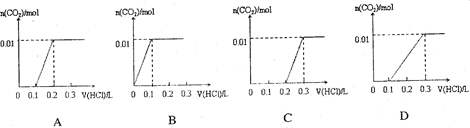
将0.4gNaOH和1.06g Na2CO3混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。下列图像能正确表示加入盐酸的体积和生成CO2的物质的量的关系的是()