下列有关实验的叙述中,正确的是( )
①仅用蒸馏水就可鉴别蔗糖、硫酸铜粉未、碳酸钙粉未;
②用分液漏斗分离甘油和水的混合物;
③稀释浓硫酸时,将浓硫酸沿烧杯壁慢慢注入水中并不断搅拌;
④用玻璃棒蘸取溶液滴在pH试纸中央,测该溶液的pH;
⑤配制一定物质的量浓度的溶液,需要的玻璃仪器只有容量瓶和烧杯;
⑥在250mL烧杯中,加入216mL水和24g NaOH固体,配制10% NaOH溶液。
| A.①⑥ | B.④⑤⑥ |
| C.①③④⑥ | D.②⑤ |
常温下,在25mL 0.1 mol·L-1 NaOH溶液中逐滴加入a mL 0.2 mol·L-1 CH3COOH溶液,有关混合溶液的判断正确的是
| A.当pH=7时,一定有:c(Na+)=c(CH3COO-)=c(OH-)=c(H+) |
| B.当a=25时,一定有:c(CH3COO-)+c(CH3COOH)=c(Na+) |
| C.当c(CH3COO-)>c(Na+)时,a一定大于12.5 |
| D.当c(OH-)>c(H+)时,a一定小于12.5 |
用铅蓄电池电解甲、乙电解池中的溶液。已知铅蓄电池的总反应为:
Pb (s)+PbO2 (s)+2H2SO4 (aq)=2PbSO4 (s)+2H2O (l),电解一段时间后向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是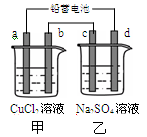
| A.d极为阴极 |
| B.放电时铅蓄电池负极的电极反应式为:PbO2 (s)+4H+(aq)+SO42-(aq)+4e-=PbSO4 (s)+2H2O (l) |
| C.若利用甲池精炼铜,b极应为粗铜 |
| D.若四个电极材料均为石墨,当析出6.4 g Cu时,两池中共产生气体3.36 L(标准状况下) |
T ℃时,在2 L的密闭容器中,X、Y、Z三种气体的物质的量随时间变化的曲线如下图所示,下列描述正确的是
| A.平衡时X、Y的转化率相同 |
B.该反应的化学方程式为:X(g)+Y(g) 2Z(g) 2Z(g) |
| C.T ℃时,若起始时X为2.00 mol,Y为2.00 mol,达平衡时Y的体积分数与原平衡Y的体积分数相同 |
| D.达到平衡后,将容器体积扩大为4 L,平衡向逆反应方向移动 |
瘦肉精学名盐酸克伦特罗,其结构简式如下图,有关瘦肉精的说法不正确的是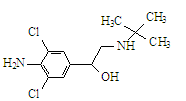
| A.化学式为C12H18ON2Cl2 |
| B.可以发生取代、加成、水解、酯化、消去反应 |
| C.属于芳香族化合物 |
| D.遇FeCl3溶液发生显色反应 |
下列离子方程式中正确的是
| A.稀硝酸和过量的铁屑反应:3Fe + 8H+ + 2NO3-=3Fe3+ + 2NO↑ + 4H2O |
B.NH4HCO3溶液与过量KOH浓溶液共热:NH4++ OH-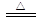 NH3↑+ H2O NH3↑+ H2O |
| C.向Ba(OH)2溶液中滴加NaHSO4溶液至恰好为中性:Ba2+ + OH- + H+ + SO42- = BaSO4↓ + H2O |
| D.KI溶液与H2SO4酸化的H2O2溶液混合:2I- + H2O2 + 2H+ =2H2O + I2 |