化学兴趣小组的同学设计实验探究浓硫酸与木炭反应后产生气体的成分。
(1)写出浓硫酸与木炭反应方程式,并标明电子转移的方向和数目:____________________。
【装置设计】组装如下的实验装置,然后进行实验探究。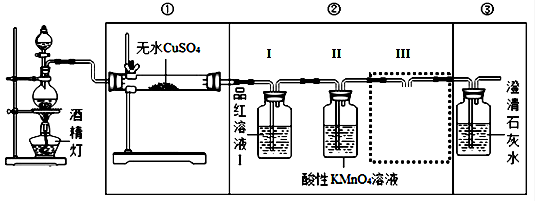
(2)装入反应物之前,必须先 。
(3)要验证产生的气体中含有CO2,请在答题卡中完成图中虚线框内的装置简图,并标明试剂。
【实验探究】
(4)观察实验,完成实验现象的部分记录:
| 实验装置 |
① |
② |
③ |
| 实验现象 |
|
…… |
|
(5)实验装置②中品红溶液Ⅰ的作用 ,III的作用 。
溴乙烷是一种难溶于水的无色液体,密度约为水的1.5倍,沸点为38.4 ℃。实验室制取溴乙烷的反应如下:
NaBr+H2SO4 NaHSO4+HBr
NaHSO4+HBr
CH3CH2OH+HBr CH3CH2Br+H2O
CH3CH2Br+H2O
已知反应物的用量,NaBr(固体)0.3 mol,乙醇0.25mol,浓硫酸36 mL(98%,密度1.84 g·cm-3),水25 mL,其中乙醇的密度约为水的密度的4/5。试回答:
(1)仅用上图所示仪器安装制取和收集溴乙烷的装置,要求达到安全、损失少、不污染环境的目的,有关仪器的选择和连接顺序为(填数字)____________。
(2)写出不能选用的仪器(填仪器代码,如甲、乙……)及理由。
| 不能选用的仪器 |
理由 |
(3)反应时,若温度过高,可见有棕色气体产生,写出反应的化学方程式:_________。
(4)从棕黄色的粗溴乙烷制取无色的溴乙烷,应加入的试剂是_________,必须使用的仪器是_______。
(5)本实验的产率为60%,则可制取溴乙烷_________g。
1,2-二溴乙烷可做抗爆剂的添加剂,常温下为无色液体,密度为2.18g cm-3,沸点131.4℃,熔点9.79℃,难溶于水,易溶于醇,醚,丙酮等有机溶剂。在实验室中可用如下图所示设备制备1,2-二溴乙烷。图中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水),据此请回答下列问题:
cm-3,沸点131.4℃,熔点9.79℃,难溶于水,易溶于醇,醚,丙酮等有机溶剂。在实验室中可用如下图所示设备制备1,2-二溴乙烷。图中分液漏斗和烧瓶a中装有乙醇和浓硫酸的混合液,试管d中装有液溴(表面覆盖少量水),据此请回答下列问题:
(1)写出制备1,2—二溴乙烷的两个反应方程式:
______________________________________、 。
(2)安全瓶b可以防止倒吸,并用于检查实验进行时试管d是否发生堵塞,请写出发生堵塞时b的现象: _________________________________________。
(3)容器c中NaOH溶液的作用是:__________________________________。
(4)某学生在做此实验时,使用一定量的液溴,当溴全部褪色时,所消耗乙醇和浓硫酸混合液的量,比正常情况下超出很多。如果装置的气密性没有问题,试分析其可能的原因 。
(5)e装置内NaOH溶液的作用是:__________________________________。
实验室制取少量溴乙烷的装置如图所示。完成下列填空:
(1)圆底烧瓶中加入的反应物是溴化钠、 和1:1的硫酸。
(2)写出加热时烧瓶中发生的主要反应的化学方程式 。
(3)将生成物导入盛有冰水混合物的试管A中,试管A中的物质分为三层(如图所示),产物在第 层。
(4)用浓硫酸进行实验,若试管A中获得的有机物呈棕黄色,除去其中杂质的正确方法是 (选填编号)。
a.蒸馏
b.氢氧化钠溶液洗涤
c.用四氯化碳萃取
d.用亚硫酸钠溶液洗涤
若试管B中的酸性高锰酸钾溶液褪色,使之褪色的有机物的名称是 。
完成以下实验:①用右图所示的装置制取溴乙烷;②进行溴乙烷的性质实验。在试管I中依次加入2 mL 蒸馏水、4 mL浓硫酸、2 mL 95%的乙醇和3g溴化钠粉末,在试管Ⅱ中注入蒸馏水,在烧杯中注入自来水。加热试管I至微沸状态数分钟后,冷却。试回答下列问题:
(1)试管I中浓硫酸与溴化钠加热反应生成氢溴酸,写出氢溴酸与乙醇在加热时反应的化学方程式 。
(2)试管I中反应除了生成溴乙烷,还可能生成的有机物有 、 (写出两种有机物的结构简式)。
(3)溴乙烷的沸点较低,易挥发,为了使溴乙烷冷凝在试管Ⅱ中,减少挥发,上图中采取的措施有 、 _。
(4)在进行溴乙烷与NaOH乙醇溶液共热的性质实验时,把生成的气体通过下图所示的装置。用下图装置进行实验的目的是 _;下图中右边试管中的现象是 ;水的作用是 。
溴乙烷在不同溶剂中与NaOH发生不同类型的反应,生成不同的反应产物。
Ⅰ:在试管中加入3 mL 1 mol/L NaOH溶液和3 mL 溴乙烷,振荡,加热。
(1)设计实验证明上述实验中溴乙烷里的Br变成了Br-
(需说明:简单的实验操作及预测产生的实验现象)。
(2)观察到 现象时,表明溴乙烷与NaOH溶液已完全反应。
(3)鉴定生成物中乙醇的结构,可用的波谱是 和 。
II:在试管中加入3 mL NaOH乙醇溶液和3 mL 溴乙烷,振荡,加热。
设计实验证明上述实验中溴乙烷发生的是消去反应
(需说明:简单的实验操作及预测产生的实验现象)。