Na2S2O3可用作照相的定影剂等。已知Na2S2O3的某些性质如下:
(1)S2O32-能被I2氧化为S4O62-; (2) 酸性条件下S2O32-迅速分解为S和SO2
Ⅰ、市售Na2S2O3中常含有SO42-, 请完成以下方案,检验其中含有的SO42-:
| 实验步骤 |
预期现象或结论 |
| 步骤1:取少量固体样品溶于无氧蒸馏水中 |
固体完全溶解得无色澄清溶液 |
| 步骤2: |
|
| 步骤3: |
|
Ⅱ、利用K2Cr2O7标准溶液可以定量测定市售硫代硫酸钠试剂的纯度,步骤为:
① 溶液配制:称取1.0gNa2S2O3试样,用新煮沸并冷却的蒸馏水溶解,最终定容至100mL。
②滴定:取10.00mL 0.01mol·L-1 K2Cr2O7标准溶液,加硫酸酸化,再加过量KI溶液。
③往步骤②所得溶液加入某指示剂,用Na2S2O3滴定至终点(2S2O32-+ I2=== S4O62-+ 2I-),记录Na2S2O3溶液用量,平行滴定3次。
(1) 步骤①中必须使用的玻璃仪器有烧杯、玻璃棒、 和 。
(2) 完成并配平步骤②中的离子反应: Cr2O72- + ( ) + I-= I2 + Cr3+ + H2O。
(3) 步骤③中,指示剂最好选用 ,该滴定应在接近中性的溶液中进行而不在强酸性溶液进行的原因是 。
(4) 若3次滴定Na2S2O3溶液的平均用量为12.00mL,则样品的纯度为 。
某实验小组用下列装置进行乙醇催化氧化的实验。
⑴实验过程中铜网出现红色和黑色交替的现象,请写出相应的化学方程式
、。
在不断鼓入空气的情况下,熄灭酒精灯,反应仍能继续进行,说明该乙醇催化反应是反应。
⑵甲和乙两个水浴作用不相同。
甲的作用是;乙的作用是。
⑶反应进行一段时间后,干燥试管a中能收集到不同的物质,它们是、、
。集气瓶中收集到的气体的主要成分是。
⑷若试管a中收集到的液体用紫色石蕊试纸检验,试纸显红色,说明液体中还含有。要除去该物质,可现在混合液中加入(填写字母)。
a.氯化钠溶液 b.苯 c.碳酸氢钠溶液 d.四氯化碳
然后,再通过 (填实验操作名称)即可得到乙醛。
⑸图中丙处导管应倾斜的原因是。
⑹本实验中若不鼓入空气,其他操作不变,乙处试管内也得到了乙醛,则发生的化学方程式为。
晶体硅是一种重要的非金属材料。制备纯硅的主要步骤如下:
①高温下用碳还原二氧化硅制得粗硅;
②粗硅与干燥HCl气体反应制得SiHCl3:Si+3HCl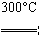 SiHCl3+H2;
SiHCl3+H2;
③SiHCl3与过量H2在1000~1100°C反应制得纯硅。
已知SiHCl3能与H2O剧烈反应,在空气中易自燃。
请回答下列问题:
(1)第①制备粗硅的化学方程式为__________________________ ____________________________________________________________________________________________________________________。
(2)粗硅与HCl反应完全后,经冷凝得到的SiHCl3(沸点33.0°C)中含有少量SiCl4(沸点57.6°C)和HCl(沸点84.7°C),提纯SiHCl3的方法为__________________________________。
(3)用SiHCl3与过量H2反应制备纯硅的装置如图所示(热源及夹持装置均已略去):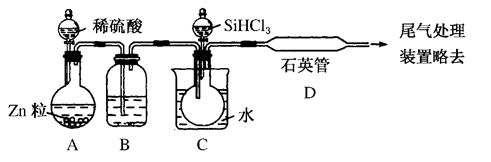
①装置B中的试剂是________,装置C中的烧瓶需要加热,其目的是__________________。
②装置D中发生反应的化学方程式为__________________________________________________________________________________________________________________________。
③为保证制备纯硅实验的成功,操作的关键是检查实验装置的气密性,控制好反应温度以及______________________________。
世界著名的科技史专家、英国剑桥大学的李约瑟博士考证说:“中国至少在距今3000年以前,就已经使用玻璃了。”下列有关普通玻璃的说法不正确的是( )
| A.制普通玻璃的原料主要是纯碱、石灰石和石英 |
| B.玻璃在加热熔化时有固定的熔点 |
| C.普通玻璃的成分主要是硅酸钠、硅酸钙和二氧化硅 |
| D.盛放烧碱溶液的试剂瓶不能用玻璃塞,是为了防止烧碱跟二氧化硅反应生成硅酸钠而使瓶塞与瓶口粘在一起 |
为确定HCl、H2CO3、H2SiO3的酸性强弱,某学生设计了如图所示的装置,一次实验即可达到目的(不必选其他酸性物质)。请据此回答: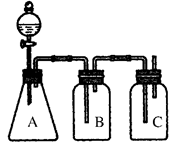
(1)锥形瓶A中装某可溶性正盐溶液,分液漏斗所盛试剂为___________________________。
(2)装置B所盛试剂是____________________,其作用是____________________________。
(3)装置C所盛试剂是________,C中反应的离子方程式是__________________________。
(4)由此可得出的结论是:酸性________>________>________。
为了讲授“氯气的性质和用途”,李老师以二氧化锰和浓盐酸为主要原料制取氯气,并设计了如图所示装置(其中A是连有注射器针头的橡皮管,针头已插入并穿过橡皮塞)进行了教学.
试回答下列问题:
(1)乙中的现象是____________________,丙中的现象是______________,丁中的现象是______________,分离丁中液体的方法是____________;
(2)橡皮管连通后,分液漏斗的气体压强p1与烧瓶中的气体压强p2的关系为________(填“>”“<”或“=”),连接橡皮管的目的是___________________________________________;
(3)烧瓶内发生反应的离子方程式为___________________________________________
________________________________________________________________________.