有一瓶澄清的溶液,其中可能含有H+、NH4+、Mg2+、Ba2+、Al3+、I-、NO3-、CO32-、SO42-、AlO2-,取该溶液进行以下实验:
(1)取pH试纸检验,溶液呈酸性,可以排除__________的存在。
(2)取出部分溶液,加入少量CCl4及数滴新制氯水,经振荡后CCl4呈紫红色,可以排除______的存在。
(3)另取出部分溶液逐滴加入NaOH溶液,使溶液由酸性逐渐变为碱性,反应过程中均无沉淀产生,则又可排除________的存在。
(4)取出部分(3)中的碱性溶液加入Na2CO3溶液,有白色沉淀生成,证明有________的存在,可以排除_____的存在。
化合物A是尿路结石的主要成分,属于结晶水合物,可用X·H2O表示。在一定条件下有如下图所示的转化关系: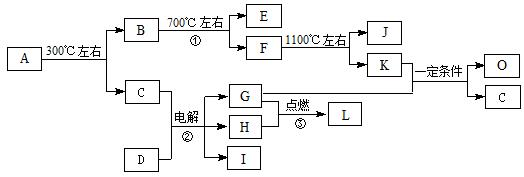
已知:
①经分析,上图中的各字母代表的物质均由常见元素(原子序数≤20)组成,其中X由三种元素组成;A、D晶体中阴、阳离子个数比都是1∶1;D中的阳离子与C分子有相同的电子数,A中的阳离子与D中的阴离子的电子层结构相同。
② G、H是常见的气体单质,E、K、L是常见的气体化合物;E被人体吸入会与血红蛋白结合而使人中毒,K的大量排放是造成地球温室效应的一个主要原因。
③反应②、③是重要的化工反应,I是一种重要的化工原料。
④上图中的部分变化经定量测定,得到如下图所示的固体产物的质量分数[ω(%)]随温度[T(℃)]的变化曲线。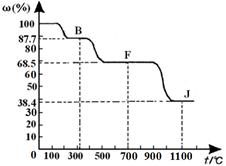
回答下列问题:
(1)写出A的化学式: ▲,D中阴离子的结构示意图为 ▲;
(2)反应①的化学方程式为: ▲。
(3)写出电解反应②的化学方程式,并标出电子转移的方向和数目: ▲。
(4)K与G在一定条件下可生成多种物质,既可获得经济效益,也减少对环境的污染。
①若O是一种易挥发的液态燃料,有毒,误饮5-10mL会导致双目失明。则O的分子式为: ▲。
②若O是K与G按1∶3的比例反应而得,则O可能是 ▲。(填编号)
A.烷烃 B.烯烃 C.炔烃 D.芳香烃
已知FeSO4在不同条件下分解得到的产物不同,可能是FeO和SO3,也可能是Fe2O3、SO3和SO2。某研究小组探究在酒精喷灯加热条件下FeSO4分解的气体产物。已知SO3的熔点是16.8℃,沸点是44.8℃。
(1)装置Ⅱ的试管中不装任何试剂,其作用是_______________________,试管浸泡在50℃的水浴中,目的是________________________________。
(2)装置Ⅲ和装置Ⅳ的作用是探究本实验气体产物成分。请完成实验设计,填写检验试剂、预期现象与结论。
限选试剂:3 mol·L-1 H2SO4、6 mol·L-1 NaOH、0.5 mol·L-1 BaCl2、0.5 mol·L-1 Ba(NO3)2、0.01 mol·L-1酸性KMnO4溶液、0.01 mol·L-1溴水。
| 检验试剂 |
预期现象和结论 |
| 装置Ⅲ的试管中加入________________。 |
产生大量白色沉淀,证明气体产物中含有SO3。 |
| 装置Ⅳ的试管中加入________________。 |
______________________________ ______________________________ ______________________________ ______________________________ |
(3)装置Ⅴ的作用是防止尾气污染环境,烧杯中应加入的试剂是。
活性氧化锌用作橡胶硫化的活性剂、补强剂。以氧化锌粗品为原料制备活性氧化锌的生产工艺流程如下: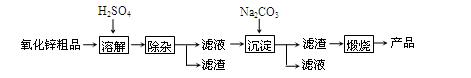
一些阳离子以氢氧化物形式完全沉淀时溶液的pH见下表:
| 沉淀物 |
Fe(OH)3 |
Cu(OH)2 |
Zn(OH)2 |
Fe(OH)2 |
| pH |
3.2 |
6.7 |
8.0 |
9.7 |
(1)“溶解”前将氧化锌粗品粉碎成细颗粒,目的是_____________________________。
(2)“溶解”后得到的酸性溶液中含有Zn2+、SO42-,另含有Fe2+、Cu2+等杂质。先加入___________(填“Na2CO3”或“H2SO4”)调节溶液的pH至5.4,然后加入适量KMnO4,Fe2+转化为Fe(OH)3,同时KMnO4转化为MnO2。经检测溶液中Fe2+的浓度为0.009mol·L-1,则每升溶液中至少应加入__________mol KMnO4。
(3)杂质Cu2+可利用置换反应除去,应选择的试剂是___________。
(4)“沉淀”得到ZnCO3·2Zn(OH)2·H2O,“煅烧”在450~500℃下进行,“煅烧”反应的化学方程式为_____________________________________。
自然界里氮的固定途径之一是在闪电的作用下,N2与O2反应生成NO。
(1)反应需要在闪电或极高温条件下发生,说明该反应_________。(填字母)
A.所需的活化能很高 B.吸收的能量很多
(2)在不同温度下,反应N2(g)+O2(g) 2NO(g)的平衡常数K如下表:
2NO(g)的平衡常数K如下表:
| 温度/℃ |
1538 |
1760 |
2404 |
| 平衡常数K |
0.86×10-4 |
2.6×10-4 |
64×10-4 |
①该反应的△H0。
(填“>”、“=”或“<”)
②其他条件相同时,在上述三个温度下分别发生该反应。1538℃时,N2的转化率随时间变化如右图所示,请补充完成1760℃、2404℃时N2的转化率随时间变化的示意图。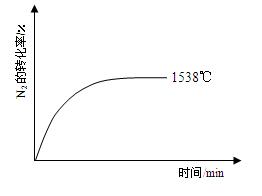
(3)2404℃时,在容积为1.0L的密闭容器中通入2.6mol N2和2.6mol O2,计算反应
N2(g)+O2(g) 2NO(g)达到平衡时NO的浓度。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
2NO(g)达到平衡时NO的浓度。(此温度下不考虑O2与NO的反应。计算结果保留两位有效数字)
化合物Ⅴ的合成路线如下(反应条件、部分生成物省略):
(1)化合物Ⅰ的分子式为 ,1 mol该物质完全燃烧需消耗 mol O2。
(2)反应①的化学方程式为________________________(不要求注明反应条件)。
(3)下列说法正确的是____________(双选,填字母)。
| A.化合物Ⅰ~Ⅴ均属于芳香烃衍生物 |
| B.反应③属于加成反应 |
| C.化合物Ⅲ和化合物Ⅴ均能使溴的四氯化碳溶液褪色 |
| D.化合物Ⅴ能与NaOH溶液反应 |
(4)反应②还会生成化合物Ⅲ的同分异构体,该同分异构体的结构简式为__________。
(5)该合成工艺中可以循环利用的有机物是_____________________。