以下物质:①NH3 ②BaCO3固体 ③酒精 ④盐酸 ⑤Cu ⑥NaCl晶体 ⑦纯醋酸
能导电的是 (填编号,下同),属于电解质的有 。
(2)9g H2O分子所含氢原子数与 L CH4(标准状况下)所含氢原子数相等;
(3)同温同压下,0.6mol O2与9.6g O3的原子个数比为 ,体积比为 。
燃料电池是一种连续的将燃料和氧化剂的化学能直接转化为电能的化学电池,除氢气外,烃、肼、甲醇等液体或气体,均可以作燃料电池的燃料。请回答下列问题:
(1)以甲烷和氧气为原料,氢氧化钠溶液为电解质溶液构成电池.写出其正极反应式
。
(2)以上述电池为电源,通过导线与图14电解池相连。
(Ⅰ)X、Y为石墨,a为1L0.1mol/L的氯化钾溶液,写出电解总反应的离子方程式
。
(II)X、Y分别为铁、铜,a为1L0.1mol/L硫酸铜溶液,写出X电极反应式
。
(3)室温时,按(I)电解一段时间后,取25mL上述电解后溶液,滴加0.2mol/L醋酸得到图15(不考虑能量损失和气体溶于水,溶液体积变化忽略不计)。
①结合图15计算消耗标准状况下甲烷mL。
②若图15的B点pH=7,则酸碱恰好完全反应的点是区间(填“AB”、“BC”或“CD”)。
③AB区间溶液中各离子浓度大小关系是。
下列框图中涉及的物质是中学化学常见的。其相互转化关系如图13所示。已知:单质A在单质G中能燃烧,其产物溶于水得 L;固体单C可以在B中燃烧;A、B、G通常为气态单质。请回答有关问题:
L;固体单C可以在B中燃烧;A、B、G通常为气态单质。请回答有关问题:
(1)写出B、L的名称:B、L;写出F在工业上的任何两点用途。
(2)写出③的化学方程式。
(3)说出形成单质C的元素在元素周期表的位置,第周期,第族。
(4)将E通入到某种棕黄色的溶液中也有L、F生成。其反应的离子方程式为
。
(5)写出④反应的化学方程式。
(16分) 现有下列三种化合物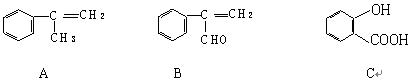
(1)请写出A经过加聚反应得到的高分子化合物的结构简式。
(2)若由A制取B,合理的反应流程是:
加成反应 → → 氧化反应 → (填相应的字母)
a.消去反应 b.水解反应 c.酯化反应 d.还原反应
(3)请写出由C生成C7H5O3Na的化学反应方程式。
(4)若 C + E  F(C11H12O4)+ H2O
F(C11H12O4)+ H2O
且
请写出③处发生反应的化学方程式;该反应类型为反应;E的结构简式为。
(5)请写出同时符合下列要求的C的所有同分异构体的结构简式
。
①含苯环②滴入FeCl3 溶液,混合液显紫色
③苯环一氯代物有两种④能发生银镜反应,不能发生水解反应
下图为中学化学中几种常见物质的转化关系(部分产物已略去)。已知:A、C、D是常见的气体单质,F气体极易溶于水,且液态常做制冷剂。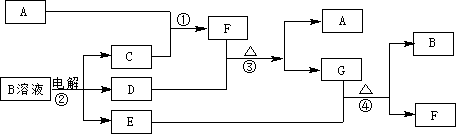
(1)写出化学式A,D,F,G属于晶体;
(2)鉴定G中阳离子的实验方法和现象_____________________________;
(3)D单质和E溶液反应,生成一种常见的消毒剂和漂白剂的有效成分,写出D+E溶液反应的离子方程式和③的化学方程式、
。
(4)常温下,电解B溶液制得pH = 12的烧碱溶液1000mL则反应中转移的电子数目为。
下表为元素周期表的一部分,请参照元素①一⑧在表中的位置,回答下列问题:
| 族 周期 |
I A |
ⅡA |
ⅢA |
ⅣA |
VA |
ⅥA |
ⅦA |
0 |
| 一 |
① |
|||||||
| 二 |
② |
③ |
④ |
|||||
| 三 |
⑤ |
⑥ |
⑦ |
⑧ |
(1)②、③、⑦的最高价含氧酸的酸性由强到弱的顺序是(写化学式)。
(2)由表中元素可以组成多种漂白剂,试写出其中两种常用漂白剂的化学式:、。
(3)①、④、⑤三种元素形成的化合物中化学键的类型:。
(4)②和④形成的化合物与④和⑤形成的化合物之间发生氧化还原反应,写出该反应的化学方程式:。
(5)由表中元素形成的常见物质X、Y、Z、M、W可发生以下反应: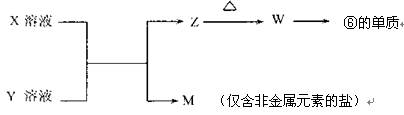
①X溶液与Y溶液反应的离子方程式为;
②已知M为硝酸盐,则M溶液中各离子浓度由大到小排列顺序为:
c()>c()>c()>c()(在括号内填离子符号)。