NA代表阿伏加德罗常数,下列叙述正确的是
| A.0.1 mol丙烯酸中含有双键的数目为0.1NA |
| B.常温常压下,Cu-Zn原电池中,正极产生1.12 L H2时,转移的电子数应为0.1NA |
C.一定条件下定容容器中充入3molH2(g)和1 mol N2(g)发生反应:H2(g)+ N2(g) 2NH3(g);△H= -QkJ/mol,当该反应放出0.25QkJ的热量时,容器中的氢分子数共有2.25 NA 2NH3(g);△H= -QkJ/mol,当该反应放出0.25QkJ的热量时,容器中的氢分子数共有2.25 NA |
| D.在50 g质量分数为46%的乙醇水溶液中,含有的氢原子总数为3NA |
下列事实不能证明HN02是弱电解质的是( )
①滴入酚酞,NaN02溶液显红色
②用HN02溶液做导电实验,灯泡很暗
③等pH、等体积的盐酸和HN02溶液中和碱时,HNO2的中和碱能力强
④0.1 mol·L-1HN02溶液的PH=2
⑤HN02与CaCO3反应放出CO2气体
⑥C(H+)="0.1" mol·L-1的HN02溶液稀释至1000倍,PH<4
| A.①⑤ | B.②⑤ | C.③⑥ | D.③④ |
用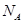 表示阿佛加德罗常数,下列说法正确的是( )
表示阿佛加德罗常数,下列说法正确的是( )
A.标准状态下22.4LS03分子数为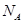 |
B.7.8gNa202含有的阴离子数是0.2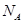 |
C.常温常压下,l6g02和16g03中所含原子数均为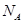 |
D.1L2mol·L-1的Al(NO3)3溶液中含Al3+个数为2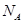 |
化学已经渗透到人类生活的各个方面,下列说法不正确的是( )
A.高铁酸钾(K2Fe04)是一种新型、高效、多功能水处 理剂,既能消毒杀菌又能净水。 理剂,既能消毒杀菌又能净水。 |
| B.“光化学烟雾”、“臭氧空洞”的形成都与氮氧化合物有关 |
C.低碳生活注重节能减排,尽量使用 太阳能等代替化石燃料,减少温室气体的排放 太阳能等代替化石燃料,减少温室气体的排放 |
| D.高纯度的硅单质广泛用于制作光导纤维.光导纤维遇强碱会“断路” |
向体积为Va的0.05 mol/L CH3COOH溶液中加入体积为Vb的0.05 mol/L KOH溶液,下列关系错误的是( )
| A.Va>Vb时:c(CH3COOH)+c(CH3COO-)>c(K+) |
| B.Va=Vb时:c(CH3COOH)+c(H+)=c(OH-) |
| C.Va<Vb时:c(CH3COO-)>c(K+)>c(OH-)>c(H+) |
| D.Va与Vb任意比时:c(K+)+c(H+)=c(OH-)+c(CH3COO-) |
下图表示的是难溶氢氧化物在不同pH下的溶解度(S,mol/L),下列说法中正确的是( )
| A.pH=3时溶液中铁元素的主要存在形式是Fe3+ |
| B.若Ni(NO3)2溶液中含有少量的Co2+杂质,可通过调节溶液pH的方法来除去 |
| C.若分离溶液中的Fe3+和Cu2+,可调节溶液的pH在4左右 |
| D.若在含有Cu2+和Ni2+的溶液中加入烧碱,Ni(OH)2优先沉淀 |