X~R是元素周期表中的短周期元素,其相关信息如下表:
| 元素 |
X |
Y |
Z |
W |
R |
| 相关信息 |
能形成+7价的化合物 |
日常生活中常见的金属,熔化时并不滴落,好像有一层膜兜着 |
通常状况下能形成短周期中最稳定的双原子分子 |
焰色反应为黄色 |
最外层有二个未成对电子,无正价 |
请用化学用语回答下列问题:
(1)基态原子X的核外电子所处最高能层的能层符号是 。
(2)Z的氢化物的电子式 ,中心原子的杂化类型是 ,元素Z、R的气体氢化物的稳定性顺序是 ,Z的氢化物易液化,原因是 。
(3)R的某种氢化物C有18个电子,工业上利用电解KHSO4水溶液所得的产物与水反应制备C。电解KHSO4水溶液时(该条件下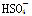 部分电离),阳极反应式是
部分电离),阳极反应式是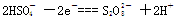 ,阴极反应式是 ;已知1mol
,阴极反应式是 ;已知1mol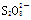 与水反应得到C时转移了2 mol e-,则该反应的离子方程式是 。
与水反应得到C时转移了2 mol e-,则该反应的离子方程式是 。
某科研小组以难溶性钾长石(K2O·Al2O3·6SiO2)为原料,提取Al2O3、K2CO3等物质,工艺流程如下:
(1)煅烧过程中有如下反应发生:
①钾长石中的硅元素在CaCO3作用下转化为CaSiO3,写出SiO2转化为CaSiO3的化学方程式:。
②钾长石中的钾元素和铝元素在Na2CO3作用下转化为可溶性的NaAlO2和KAlO2,写出Al2O3转化为NaAlO2的化学方程式:。
(2)已知NaAlO2和KAlO2易发生如下水解反应:AlO2-+ 2H2O Al(OH)3+ OH-。“浸取”时应保持溶液呈________性(填“酸”或“碱”),“浸取”时不断搅拌的目的是_________。
Al(OH)3+ OH-。“浸取”时应保持溶液呈________性(填“酸”或“碱”),“浸取”时不断搅拌的目的是_________。
(3)“转化”时加入NaOH的主要作用是(用离子方程式表示)_________。
(4)上述工艺中可以循环利用的主要物质是________、________和水。
化工工业中常用乙苯脱氢的方法制备苯乙烯。已知某温度下:
反应①:CO2(g)+H2(g) CO(g)+H2O(g),ΔH=" +41.2" kJ/mol;
CO(g)+H2O(g),ΔH=" +41.2" kJ/mol;
反应②: (g)
(g)
 (g)+H2(g),ΔH=" +117.6" kJ/mol。
(g)+H2(g),ΔH=" +117.6" kJ/mol。
①、②的化学反应平衡常数分别为K1、K2。
(1)请写出二氧化碳氧化乙苯制备苯乙烯的热化学反应方程式。该反应的化学平衡常数K=(用K1、K2表示)。
(2)恒温恒容条件下,反应①达到平衡后,t1时刻通入少量CO2。请
画出t1之后的正逆反应曲线,并作出标注。
(3)已知某温度下,Ag2SO4饱和溶液中c(Ag+)="0.04" mol/L,则该温度
下Ksp(Ag2SO4)=。(保留两位有效数字)
(4)电解法制备高铁酸钠(Na2FeO4),总反应式为:Fe+2H2O+2OH-=FeO42-+3H2↑,电解质溶液选用NaOH溶液。该电解池阳极材料是(写化学式);阳极的电极反应式为__ _________。
香兰素( )是食品添加剂的增香原料,其合成路线如下:
)是食品添加剂的增香原料,其合成路线如下:

(1)写出A的结构简式,反应③的反应类型是______________。
(2)写出反应④的化学方程式_______________________________(不用注明条件)。
(3)1 mol香兰素在一定条件下与H2发生反应,最多消耗H2_________mol。
(4)D与香兰素互为同分异构体,能与NaHCO3溶液反应放出气体,遇FeCl3溶液显紫色,且苯环上的一氯取代物只有2种,请写出D的结构简式_________。
(5)香兰素的另一种同分异构体结构简式为 ,在一定条件下可以合成聚酯高分子,写出该聚酯高分子的结构简式__________。
,在一定条件下可以合成聚酯高分子,写出该聚酯高分子的结构简式__________。
钢铁企业酸洗钢材时产生的废液主要成分为Fe2+、H+、Cl-,可用下述方法处理该废液,回收盐酸和制备氧化铁涂料。 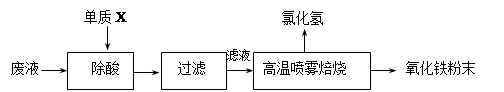
(1)单质X的化学式是。
(2)氯化亚铁溶液经高温喷雾焙烧转化为HCl气体和氧化铁粉末,有关的化学方程式依次为:。
(3)某铁红涂料中除含有Fe2O3外,还可能添加有CuO或FeO中的一种,请设计实验方案,探究该铁红涂料中添加物的成分。
① 提出合理假设
假设1:添加了CuO
假设2:添加了FeO
② 请设计方案,验证上述假设,写出实验步骤、预期现象和结论。
限选试剂:铁粉、3mol•L-1H2SO4、0.1 mol•L-1酸性KMnO4溶液、10%NaOH溶液、10%H2O2、KSCN溶液
| 操作步骤 |
预期现象和结论 |
| 步骤1.取少量样品于试管中, ____________________________________________ |
样品全部溶解,得到澄清的溶液。 |
| 步骤2. 步骤3. |
___________________________ ___________________________ |
(4)请计算,用635g水完全吸收“高温喷雾焙烧”产生的HCl气体升(标准状况),即可得到36.5%的浓盐酸(相对原子质量 Cl 35.5 H 1)。
高纯六水氯化锶晶体(SrCl2·6H2O)具有很高的经济价值,工业上用难溶于水的碳酸锶(SrCO3)为原料(含少量钡和铁的化合物等),制备高纯六水氯化锶晶体的过程为:
已知: Ⅰ. SrCl2·6H2O 晶体在61℃时开始失去结晶水,100℃时失去全部结晶水。
Ⅱ.有关氢氧化物开始沉淀和完全沉淀的pH表:
| 氢氧化物 |
Fe(OH)3 |
Fe(OH)2 |
| 开始沉淀的pH |
1.5 |
6.5 |
| 沉淀完全的pH |
3.7 |
9.7 |
(1)操作①加快反应速率的措施有(写一种)。
碳酸锶与盐酸反应的离子方程式。
(2)酸性条件下,加入30% H2O2溶液,将Fe2+氧化成Fe3+,其离子方程式为。
(3)在步骤②-③的过程中,将溶液的pH值由1调节至4时,宜用的试剂为_______。
A.氨水 B.氢氧化锶粉末 C. 氢氧化钠 D.碳酸钠晶体
(4)操作③中所得滤渣的主要成分是(填化学式)。
(5)步骤④的操作是、。
(6)工业上用热风吹干六水氯化锶,适宜的温度是
A.50~60℃ B.70~80℃ C.80~100℃ D.100℃以上