甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g)  CH3OH(g)下表为不同温度下的平衡常数(K)
CH3OH(g)下表为不同温度下的平衡常数(K)
| 温度 |
250℃ |
300℃ |
350℃ |
| K |
2.041 |
0.270 |
0.012 |
(1)该反应的平衡常数表达式K= ,ΔH 0(填“>”、“<”或“=”)。
(2)将1 mol的H2和 1 mol 的 CO充入 1 L 恒容密闭反应器中,达到平衡后,容器内的压强为开始时的60%,求CO的平衡转化率(写出计算过程)。
(3)300℃时,将容器的容积压缩到原来的1/2,在其他条件不变的情况下,对平衡体系产生的影响是
(填字母)。
A.c(H2)减少
B.正反应速率加快,逆反应速率减慢
C.CH3OH 的物质的量增加
D.重新平衡时c(H2)/ c(CH3OH)减小
(4)其他条件相同时,在上述三个温度下分别发生该反应。300℃时,H2的转化率随时间的变化如图所示,请补充完成350℃时H2的转化率随时间的变化示意图。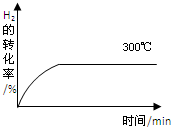
(1)25℃时,一定浓度的K2Cr2O7溶液中存在下列平衡:Cr2O72-(橙红色)+H2O  2CrO42-(黄色)+2H+K=8.3×10-15,则该反应的平衡常数表达式为
2CrO42-(黄色)+2H+K=8.3×10-15,则该反应的平衡常数表达式为
K=
取少量上述溶液两等份,分别滴加浓硫酸和浓烧碱溶液,出现的现象依次是,
(2)已知在T=298K时,反应:2H2O2(l)=2H2O(l)+O2(g) △H =" –196.5" kJ/mol
则该正向反应的△S0,
令△G=△H-T△S ,判断该正向反应的△G0 ,自发进行(填“能”或“不能”)
研究表明:过氧化氢酶对上述反应的催化效果最佳,这是由于它能极大地降低该反应的 。
(3)向K2Cr2O7酸性溶液中加入H2O2,能生成深蓝色的过氧化铬CrO(O2)2反应如下:Cr2O72-+4H2O2+2H+=2CrO(O2)2+5H2O
类比于Na2O2,判断:该反应 (填“属于”或“不属于”)氧化还原反应,过氧化铬中铬元素的化合价为
硝基苯甲酸乙酯在OH-存在下发生水解反应:O2NC6H4COOC2H5+ OH- O2NC6H4COO-+C2H5OH
O2NC6H4COO-+C2H5OH
两种反应物的初始浓度均为0.050mol/L,15 ℃时测得:O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示。
| t/s |
0 |
120 |
180 |
240 |
330 |
530 |
600 |
700 |
800 |
| α/% |
0 |
33.0 |
41.8 |
48.8 |
58.0 |
69.0 |
70.4 |
71.0 |
71.0 |
回答下列问题:
(1)计算上述反应在120~180s与180~240s区间的平均反应速率
v1= 、v2= 。
比较两者大小可得到的结论是。
(2)列式计算15 ℃时该反应的平衡常数K=_________________。(填数值)
(3)为提高反应物的平衡转化率,除适当控制反应温度外,另可采取的措施有,(要求写出两条)。
氮元素在地球上丰度较大,氮及其化合物用途广泛。请回答:
(1)下图是氮气和氢气反应生成1mol氨气的能量变化示意图,写出上述反应的热化学方程式: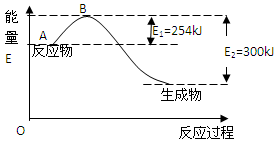
(2)已知下列数据:
| 化学键 |
H—H |
N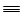 N N |
| 键能/( kJ/mol) |
435 |
943 |
根据表中和图中数据,计算N-H的键能为:kJ/mol
(3)用氨催化还原NOx(氮氧化物),可消除污染。
已知:4NH3(g)+3O2(g) =2N2(g)+6H2O(g) △H1 =" –a" kJ/mol
N2(g)+O2(g)=2NO(g)△H2 =" –b" kJ/mol
则反应:4NH3(g)+6NO(g)=5N2(g)+6H2O(g)的反应热△H=kJ/mol(用含a和b的代数式表示)其中氧化剂是,还原剂是(均填分子式)
实验题
(1)为准确测定中和热,除了提供的酸和碱溶液的浓度与体积必须准确外,在实验过程中的另外两个重要措施是:、
(2)在草酸溶液中加入酸性高锰酸钾溶液,发生如下反应。请配平: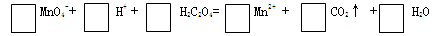
该反应开始时速率较慢,但一段时间后,紫色突然褪去,其主要原因是:。
(3)人们常常根据反应的特征现象来判断反应进行的快慢。对于下列反应:Na2S2O3 + H2SO4 =Na2SO4+S+SO2+H2O 通常测定在一定条件下单位时间内出现(明显)现象来比较该反应进行的快慢。为增大上述反应的速率,可采取的不同措施有:,。
已知下列反应:
①2C(s)+O2(g)=2CO(g)△H1 =" –221" kJ/mol
②CO(g)+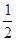 O2(g)=CO2 (g)△H2 =" –283" kJ/mol
O2(g)=CO2 (g)△H2 =" –283" kJ/mol
③ 稀溶液中:H+(aq)+OH-(aq)=H2O(l)△H3 =" –57.3" kJ/mol
请回答下列问题:
(1)碳(C)的燃烧热为。
已知碳的两种同素异形体的转化:C(s,金刚石) = C(s,石墨) △H =" –1.9" kJ/mol
则从能量角度判断:稳定性更大的是(填名称)
(2)写出能表达反应③意义的一个热化学方程式
若稀醋酸与氢氧化钠稀溶液恰好反应的中和热为△H4,则△H3△H4(填“>”,“=”或“<”)