现有五种可溶性物质A、B、C、D、E,它们所含的阴、阳离子互不相同,分别含有五种阳离子Na+、Al3+、Mg2+、Ba2+、Fe3+和五种阴离子Cl–、OH–、NO3–、CO32–、Xn-中的一种。
(1)某同学通过分析比较,认为无需检验就可判断其中必有的两种物质是
和 (填化学式)。
(2)为了确定Xn–,现将(1)中的两种物质记为A和B,当C与B的溶液混合时,产生红褐色沉淀和无色无味气体;当C与A的溶液混合时产生混合物沉淀,向该沉淀中滴入稀盐酸,沉淀部分溶解,最后仍有白色沉淀不再溶解。则:
①Xn-为 (填序号)。
A.SO32– B.SO42– C.CH3COO– D.SiO32–
②写出物质C与B反应的离子反应式
③将0.2mol的A与0.1mol的C同时溶解在足量的蒸馏水中,充分反应后,最终所得沉淀的物质的量为 mol。
④利用上述已经确定的物质 (填化学式),可以检验出D、E中的阳离子。
、
、
、
、
、
、
、
、
是中学化学中常见的气体,它们均由短周期元素组成,具有如下性质:
①
、
、
、
、
能使湿润的蓝色石蕊试纸变红,
能使湿润的红色石蕊试纸变蓝,
、
、
不能使湿润的石蕊试纸变色;
②
和
相遇产生白色烟雾;
③
和
都能使品红溶液褪色;
④将红热的铜丝放入装有
的瓶中,瓶内充满棕黄色的烟;
⑤将点燃的镁条放入装有
的瓶中,镁条剧烈燃烧,生成白色粉末,瓶内壁附着黑色颗粒;
⑥
和
相遇生成红棕色气体;
⑦G在
中燃烧可以产生
和
;
⑧将
和
在瓶中混合后于亮处放置几分钟,瓶内壁出现油状液滴并产生
。
回答下列问题:
(1)
的化学式是,②中烟雾的化学式是;
(2)④中发生反应的化学方程式是 ;
;
(3)⑤中发生反应的化学方程式是;
(4)
的化学式是,
的化学式是;
(5)⑦中发生反应的化学方程式是;
(6)
的化学式是。
向2L密闭容器中通入a
气体
和b
气体B,在一定条件下发生反应;

已知:平均反应速率
;反应2
时,
的浓度减少了
,B的物质的量减少了
,有
生成。
回答下列问题:
(1)反应2
内,
=,
=;
(2)化学方程式中,
、
、
、
;
(3)反应平衡时,
为2a
,则
的转化率为;
(4)如果只升高反应温度,其他反应条件不变,平衡时D为1.5
,则该反应的
0;(填">"、"<"或"=")
(5)如果其他条件不变,将容器的容积变为1
,进行同样的实验,则与上述反应比较:
①反应速率(填"增大"、"减小"或"不变"),理由是;
②平衡时反应物的转化率(填"增大"、"减小"或"不变"),理由是;
(15分)有机化合物A~H的转换关系如下所示: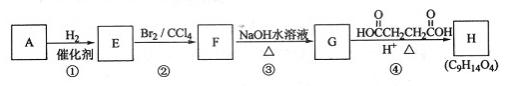
请回答下列问题:
(1)链烃A有南链且只有一个官能团,其相对分子质量在65~75之间,1 mol A完全燃烧消耗7 mol氧气,则A的结构简式是 ,名称是 ;
(2)在特定催化剂作用下,A与等物质的量的H2反应生成E。由E转化为F的化学方程式是 ;
(3)G与金属钠反应能放出气体,由G转化为H的化学方程式是 ;
(4)①的反应类型是 ;③的反应类型是 ;
(5)链烃B是A的同分异构体,分子中的所有碳原子共平面,其催化氢化产物为正戊为烷,写出B所有可能的结构简式
(6)C也是A的一种同分异构体,它的一氯代物只有一种(不考虑立体异构,则C的结构简式为 。
请设计CO2在高温下与木炭反应生成CO的实验。
(1)在下面方框中,A表示有长颈漏斗和锥形瓶组成的气体发生器,请在答题卡上的A后完成该反应的实验装置示意图(夹持装置,连接胶管及尾气处理不分不必画出,需要加热的仪器下方用△标出),按气流方向在每件仪器下方标出字母B、C……;其他可选用的仪器(数量不限)简易表示如下:
(2)根据方框中的装置图,在答题卡上填写该表
| 仪器符号 |
仪器中所加物质 |
作用 |
| A |
石灰石、稀盐酸 |
石灰石与盐酸生成CO2 |
(3)有人对气体发生器作如下改进:在锥形瓶中放入一小试管,将长颈漏斗下端插入小试管中。改进后的优点是 ;
(4)验证CO的方法是 。
有A、B、C、D、E和F六瓶无色溶液,他们都是中学化学中常用的无机试剂。纯E为无色油状液体;B、C、D和F是盐溶液,且他们的阴离子均不同。现进行如下实验:
①A有刺激性气味,用沾有浓盐酸的玻璃棒接近A时产生白色烟雾;
②将A分别加入其它五中溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化,F中沉淀完全溶解;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶。
根据上述实验信息,请回答下列问题:
(1)能确定溶液是(写出溶液标号与相应溶质的化学式):
(2)不能确定的溶液,写出其标号、溶质可能的化学式及进一步鉴别的方法: