NA表示阿伏加德罗常数的值,下列说法正确的是
| A.1molCl2参加的任何反应转移电子数都是2NA |
| B.1mol/L的NaCl溶液中含有NA个Na+ |
| C.标准状况下,22.4ml水中含有的分子数约为1.24NA |
| D.1molFeCl3完全水解生成NA个胶体粒子 |
下列关于有机物的说法中,不正确的是:
| A.糖类、油脂和蛋白质都能发生水解反应 |
| B.乙烯、氯乙烯均可用于合成塑料 |
| C.甲烷、苯、乙醇和乙酸在一定条件下都能发生取代反应 |
| D.分子式为C6H14的有机物只有5种,它们属于同分异构体 |
下列各组热化学方程式中,化学反应的△H前者大于后者的是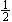 ①C(s)+O2(g)=CO2(g);△H1C(s)+O2(g)="CO(g);" △H2
①C(s)+O2(g)=CO2(g);△H1C(s)+O2(g)="CO(g);" △H2
②2H2(g)+O2(g)=2H2O(g); △H3 2H2(g)+O2(g)=2H2O(1);△H4
③CaCO3(s)=CaO(s)+CO2(g); △H5 CaO(s)+H2O(1)=Ca(OH)2(s);△H6
| A.①② | B.①③ | C.②③ | D.只有② |
某温度下, 的平衡常数
的平衡常数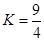 .该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是
.该温度下在甲、乙、丙三个恒容密闭容器中,投入H2(g)和CO2(g),其起始浓度如表所示。下列判断不正确的是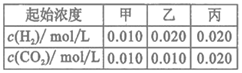
| A.平衡时,乙中CO2的转化率大于60% |
| B.平衡时,甲中和丙中H2的转化率均是60% |
| C.平衡时,丙中c(CO2)是甲中的2倍,是0.012mol/L |
| D.反应开始时,丙中的反应速率最快,甲中的反应速率最慢 |
下列各组离子一定能大量共存的是
| A.含有大量硝酸根离子的溶液中H+、Fe2+、SO42-、Cl- |
| B.c(H + )/c(OH - ) = 1×10-10的溶液中NH4+、K+、Ca2+、Cl- |
| C.加入铝粉有氢气产生的溶液中Na+、K+、SO42-、Cl- |
D.水电离的c(H + ) = 1×1 0-12mol/L 的溶液中Na+、K+、HCO-3、Cl- 0-12mol/L 的溶液中Na+、K+、HCO-3、Cl- |
下列反应的离子方程式正确的是
| A.铜片插入氯化铁溶液中 Cu+Fe3+=Cu2++Fe2+ |
B.电解饱和食盐水 2Cl—+2H+ 2Cl—+2H+ H2↑+C12↑ H2↑+C12↑ |
C.向溴化亚铁溶液中通入过量的氯气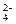 2Fe2++Cl2=2Fe3++2Cl- 2Fe2++Cl2=2Fe3++2Cl- |
| D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加足量Ba(OH)2溶液 |
NH4++Al3++2SO42—+2Ba2++5OH-=AlO2-+2BaSO4↓+NH3·H2O+2H2O