某化学兴趣小组利用下图装置探究制取气体的原理、方法及性质。结合装置图,回答下列问题:
(1)写出仪器的名称a b 。收集某气体只能用D装置,由此推测该气体具有的性质是 、 ;
(2)用大理石和稀盐酸制取二氧化碳时,可选用的发生与收集装置是 (填上图字母) ,化学方程式是 。
(3)该小组设计了如下图所示的实验装置,既可用于制取气体,又可用于探究物质性质。
①当打开K1、关闭K2时,利用I、Ⅱ装置,可进行的实验是 (填字母)。
a.大理石与稀盐酸反应制取二氧化碳
b.锌与稀硫酸反应制取氢气
②当打开K2、关闭K1时,可以利用工、Ⅲ装置制得二氧化碳并验证其性质。为了进一步验证产生的气体是二氧化碳,该同学将气体通入Ⅲ中,则该装置中应加入的试剂为 (填化学式)。若在f装置中加入紫色石蕊试液,观察到的现象是 。得出的结论是 。(用化学方程式表达)
某校化学兴趣小组就空气中氧气的含量进行实验探究: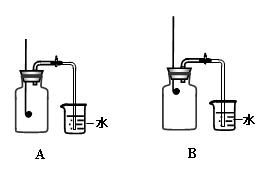
[集体讨论]
(1)讨论后同学们认为,选择的药品既要能消耗氧气,又不会跟空气中的其它成分反应,而且生成物为固体。他们应该选择(填编号),
A.蜡烛 B.红磷 C.硫粉
为了充分消耗容器中的氧气,药品的用量应保证。
(2)小组同学共同设计了如上图的两套装置,你认为合理的是(填编号)。
为了确保实验的成功,在装药品之前应该。
[分组实验]在讨论的基础上,他们分组进行了实验。
[数据分析]实验结束后,整理数据如下:(注:集气瓶容积为100mL)
| 组别 |
1 |
2 |
3 |
4 |
5 |
6 |
| 进入集气瓶中水的体积(mL) |
20 |
21 |
19 |
20 |
22 |
18 |
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的。
通过实验还可以推断集气瓶中剩余气体是。
[实验拓展]
(4)小组的同学做完实验后又尝试用木炭重新做了以上实验,发现水几乎没有进入集气瓶。经讨论,同学们一致认为如果事先在集气瓶内注入少量碱溶液来吸收木炭燃烧产生的气体,实验也能取得较好的效果。
以下是某研究小组探究影响化学反应快慢的一些因素的相关数据(常温通常指20℃;“浓度”指溶质的质量分数)
| 实验序号 |
过氧化氢溶液浓度/% |
过氧化氢溶液质量/g |
温度/℃ |
二氧化锰用量/g |
氧气体积/ml |
反应所需时间/s |
| ① |
5 |
12 |
20 |
0.2 |
125 |
11 |
| ② |
30 |
12 |
20 |
0.2 |
125 |
2 |
| ③ |
30 |
12 |
40 |
/ |
125 |
148 |
| ④ |
30 |
12 |
90 |
/ |
125 |
82 |
(1)通过实验①和②对比可知,化学反应快慢与有关,其关系是。
(2)通过对比实验和可知,化学反应快慢与温度的关系是。
(3)除了上述的两个因素能影响化学反应快慢,你认为另一个影响因素是什么,其关系是怎样的?。
(4)由上述实验可知,实验室用过氧化氢制取氧气的最合适的条件是
。
有空气、氧气、二氧化碳三种无色气体如何一次性将它们鉴别出来,请写出操作方法、现象、结论。
用来测定空气成分的方法很多,如图所示是小明用红磷在空气中燃烧的测定方法。实验过程是: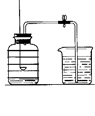
第一步:将集气瓶容积划分为五等份,并做好标记。
第二步:点燃燃烧匙内的红磷,伸入集气瓶中并把塞子塞紧。
第三步:待红磷熄灭并冷却后,打开弹簧夹,发现水被吸
入集气瓶中,进入集气瓶中水的体积约为集气瓶总容积的1/5。
请回答下列问题:
(1)上面的实验同时证明了氮气有的化学性质。
(2)实验完毕,若进入集气瓶中水的体积不到总容积的1/5,你认为导致这一结果的原因可能是。(至少二点)
(3)某同学选用木炭代替红磷进行实验,是否可行?为什么?
探究实验报告一:蜡烛及其燃烧的探究
探究实验的名称:蜡烛及其燃烧的探究
探究实验的目的:理解掌握蜡烛的有关性质知识
实验用品:蜡烛、火柴、等
| 步骤和方法 |
现象 |
分析 |
|
| 点燃前[ |
蜡烛是白色蜡状固体,硬度小,稍有气味 |
||
| 用小刀切下一小块蜡烛投入水中 |
石蜡浮于水面 |
||
| 点燃蜡烛 |
蜡烛先熔化后气化,再燃烧;火焰明亮且明显分成三层 |
||
| 在烛焰上方罩一干燥烧杯 |
烧杯内壁出现水雾或水珠 |
||
| 在烛焰上方罩一个内壁沾有澄清石灰水的烧杯,振荡 |
烧杯内壁出现白色斑点 |
||
| 熄灭蜡烛 |
火焰熄灭,灯芯上产生一缕轻烟 |
轻烟为蜡烛蒸气冷却所致,遇明火可以燃烧。 |
结论:在通常情况下,蜡烛是白色蜡状固体,稍有气味,熔点、熔点较低,硬度较小,密度比水小。蜡烛在点燃条件下能燃烧,燃烧产物中有水和二氧化碳等。
问题和建议:为进一步说明蜡烛是先气化,然后是石蜡蒸气燃烧,可用一根尖嘴的细玻璃管插入焰心,然后在尖嘴处点燃。根据是否能点燃,可推断上述猜测是否正确。