(本题10分)电化学在工业生产中有广泛应用。
(1)下图所示装置中,两玻璃管及烧杯中是滴有酚酞的NaCl饱和溶液C(Ⅰ)、C(Ⅱ)为多孔石墨电极。
①电解NaCl饱和溶液的化学方程式为:_________________________。
②接通S1后,C(Ⅰ)附近溶液变红,两玻璃管中均有气体生成。则电极C(Ⅰ)是_________(填“阳”或“阴”);C(Ⅱ)电极反应所得气体产物为_________。
③通电一段时间后(玻璃管中液面未脱离电极),断开S1,接通S2,电流表的指针发生偏转,此时电极C(Ⅰ)为_________(填“正”或“负”)极;C(Ⅰ)的电极反应为:______________________________________。
(2)若用此装置精炼粗铜,断开S2,接通S1,电解液选用CuSO4溶液;粗铜接电池的_________(填“正”或“负”)极,阴极发生的电极反应为:_____________________________。
[化学—选修3:物质结构与性质](15分)已知A、B、C、D、E五种元素的原子序数依次增大,其中A原子所处的周期数、族序数都与其原子序数相等;B原子核外电子有6种不同的运动状态,s轨道电子数是p轨道电子数的两倍;D原子L电子层上有2对成对电子;E+原子核外有3层电子且各层均处于全满状态。
请填写下列空白。
(1)E元素基态原子的核外电子排布式为_________________。
(2)B、C、D三种元素的第一电离能数值由小到大的顺序为_____________(填元素符号),其原因为_____________________。
(3)B元素的最高价氧化物对应的水化物中心原子采取的轨道杂化方式为 ,C元素的气态氢化物的VSEPR模型为 。B2A4是重要的基本石油化工原料,1 mol B2A4分子中含__________molσ键。
(4)B元素可形成多种单质,一种晶体结构如图一所示;另一种的晶胞如图二所示,该晶胞的空间利用率为 (保留两位有效数字)。( )
)
(5)向E的硫酸盐溶液中滴加过量氨水,观察到的现象是 。请写出上述过程的离子方程式 。
[化学一选修2:化学与技术](15分)合成氨的流程示意图如下: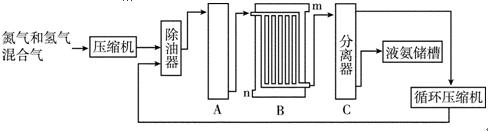
回答下列问题:
(1)工业合成氨的原料是氮气和氢气。氮气是从空气中分离出来的,通常使用的两种分离方法是________、________;氢气的来源是水和碳氢化合物,写出分别采用煤和天然气为原料制取氢气的化学反应方程式__________________________,______________________。
(2)设备A中含有电加热器、触媒和热交换器,设备A的名称是________,其中发生的化学反应方程式为___________;
(3)设备B的名称是________,其中m和n是两个通水口,入水口是________(填“m”或“n”)。不宜从相反方向通水的原因是______________________________;
(4)设备C的作用是_____________________________;
(5)在原料气制备过程中混有的CO对催化剂有毒害作用,欲除去原料气中的CO,可通过如下反应来实现:
CO(g)+H2O(g) CO2(g)+H2(g)。已知1 000 K时该反应的平衡常数K=0.627,若要使CO的转化率超过90%,则起始物中c(H2O)∶c(CO)不低于________。
CO2(g)+H2(g)。已知1 000 K时该反应的平衡常数K=0.627,若要使CO的转化率超过90%,则起始物中c(H2O)∶c(CO)不低于________。
(13分)运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义。
(1)硫酸生产过程中2SO2(g)+O2(g) 2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图所示,根据如图回答下列问题:
2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图所示,根据如图回答下列问题: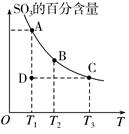
①2SO2(g)+O2(g) 2SO3(g)的ΔH________0(填“>”或“<”)。
2SO3(g)的ΔH________0(填“>”或“<”)。
②一定条件下,将SO2与O2以体积比为2∶1置于一体积不变的密闭容器中发生以下反应,能说明该反应已达到平衡的是________(填选项字母)。
a.体系的密度不发生变化
b.SO2与SO3的体积比保持不变
c.体系中硫元素的质量分数不再变化
d.单位时间内转移4 mol电子,同时消耗2 mol SO3
e.容器内的气体分子总数不再变化
(2)一定条件下,合成氨反应为:N2(g)+3H2(g) 2NH3(g)。图1表示在此反应过程中的能量变化,图2表示在2 L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量变化,图2表示在2 L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。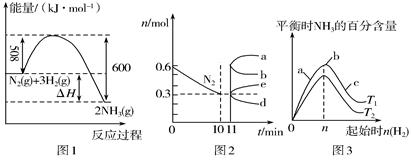
①该反应的平衡常数表达式为________,升高温度,平衡常数________(填“增大”“减小”或“不变”)。
②由图2信息,计算0-10 min内该反应的平均速率v(H2)________,从11 min起其他条件不变,压缩容器的体积为1 L,则n(N2)的变化曲线为________(填“a”“b”“c”或“d”)。
③图3 a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是________点,温度T1________T2(填“>”“=”或“<”)。
【化学:选修5-有机化学基础】香料V的制备方法如下:
(1)化合物Ⅰ的分子式为________,Ⅳ中含氧官能团的名称是________。
(2)化合物Ⅰ可由 经两步反应制得,写出第一步反应的化学方程式______________。
经两步反应制得,写出第一步反应的化学方程式______________。
(3)1 mol的化合物Ⅱ和Ⅲ分别与H2反应,最多消耗H2的物质的量之比为________。
(4)该工艺中第①步的目的是_____________________________________________________。
为检验①中CH3I的碘原子,实验室的操作是取少量CH3I于试管中,加入足量的NaOH水溶液,加热充分反应,冷却后加入________,再加入少量硝酸银溶液。
(5)芳香化合物Ⅵ是Ⅲ的一种无甲基异构体,能发生水解反应和银镜反应,Ⅵ的结构简式为________。
(6)一定条件下,化合物Ⅳ与乙二醇发生类似反应④的反应,该反应有机产物的结构简式为________。
【化学:选修3—物质结构与性质】前四周期元素X、Y、Z、W、R的原子序数依次增大,已知:X原子的2p轨道为半充满状态;Y原子的L层有2个未成对电子;Z与Y位于同主族;W的+2价简单离子核外电子层排布与Ar原子相同;R原子的d轨道上有3个空轨道。请回答下列问题:
(1)R原子的基态电子排布式为 。
(2)X、Y原子的第一电离能大小顺序为 。(用元素符号表示)
(3)X的常见单质分子结构中σ键数目为 。
(4)X元素的气态氢化物的VSEPR模型为 。Z的最高价氧化物对应水化物的酸根离子空间构型为 ,中心原子的杂化轨道类型为 。
(5)某矿物晶体由Y、W、R三种元素组成,其晶胞结构如图所示。
则该矿物的化学式为 ,若已知该晶胞的边长为a cm,则该晶胞的密度为 g/cm3。(用含a、NA的代数式表示)