金属钒(V)在材料科学上有重要作用,被称为“合金的维生素”。以下是测定矿石中钒的含量的两个反应:
(1)用稀硫酸溶解五氧化二钒(V2O5),得到(VO2)2SO4溶液。写出该反应的化学方程式_________________;
该反应______(选填“是”或“不是”)氧化还原反应。
(2)用已知浓度的硫酸酸化的H2C2O4溶液,滴定(VO2)2SO4溶液,完成下列离子方程式,方框内填
数字,短线上填写物质的化学式或离子符号。
VO2+ + H2C2O4 + ______ → VO2+ + CO2 ↑ + ______
(3)当收集到标准状况下气体11.2L时,转移的电子数目为 。
(4)甲同学提出:上述反应能否用盐酸酸化?乙同学认为:要回答这个问题还得知道 。
A.VO2+和HCl氧化性相对强弱
B.VO2+和Cl2氧化性相对强弱
C.上述均不正确
现有下列物质:①乙炔 ②苯酚溶液 ③乙醛 ④淀粉溶液 ⑤氨基酸。请回答:
(1)遇碘水呈蓝色的是 (填序号,下同)。
(2)能发生成肽反应的是 。
(3)能跟溴发生加成反应的是 。
(4)能跟银氨溶液发生银镜反应的是 。
(5)能跟饱和溴水反应生成白色沉淀的是 。
1915年诺贝尔物理学奖授予Henry Bragg和Lawrence Bragg,以表彰他们用X射线对晶体结构的分析所作的贡献.
(1)科学家通过X射线探明,NaCl、KCl、MgO、CaO晶体结构相似,其中三种晶体的晶格能数据如下表:
| 晶体 |
NaCl |
KCl |
CaO |
| 晶格能/(kJ•mol-1) |
786 |
715 |
3401 |
四种晶体NaCl、KCl、MgO、CaO熔点由高到低的顺序是__________,Na、Mg、Al第一电离能I1从小到大的排列顺序是____________。
(2)科学家通过X射线推测胆矾中既含有配位键,又含有氢键,其结构示意图可简单表示如图,其中配位键和氢键均采用虚线表示。
①实验证明,用蒸汽密度法测得的H2O的相对分子质量比用化学式计算出来的相对分子质量要大,其原因是_________________。
②SO42-中S原子的杂化类型是,与其互为等电子体的分子有________(任写一种)。
③Cu2+还能与NH3、Cl-等形成配位数为4的配合物,[Cu(NH3)4]2+中存在的化学键类型有__(填序号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
④写出基态Cu原子的外围电子排布式;金属铜采用面心立方堆积方式,已知Cu原子的半径为r pm,相对原子质量为M,NA表示阿伏加德罗常数,则金属铜的密度是_____g/cm3(列出计算式)。
2015年8月12日23:30左右,天津滨海新区的一处集装箱码头发生爆炸,发生爆炸的是集装箱内的易燃易爆物品氰化钠,数量为700吨左右。
资料:氰化钠化学式为NaCN,白色结晶颗粒或粉末,易潮解,有微弱的苦杏仁气味。剧毒,皮肤伤口接触、吸入、吞食微量可中毒死亡。熔点563.7℃,沸点1496℃。易溶于水,易水解生成氰化氢,水溶液呈强碱性,是一种重要的化工原料, 用于电镀、冶金和有机合成医药、农药及金属处理方面。
(1)用离子方程式表示其水溶液呈强碱性的原因:_________________。
(2)氰化钠要用双氧水或硫代硫酸钠中和。①用双氧水处理产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,请写出该反应的化学方程式 ;
②用硫代硫酸钠中和的离子方程式为CN-+S2O32-=A+SO32-,A为 (填化学式)。
(3)含氰废水中的CN-有剧毒。
①CN-中C元素显+2价, N元素显-3价,则非金属性N C(填<,=或>)
②在微生物的作用下,CN-能够被氧气氧化成HCO3-,同时生成NH3,该反应的离子方程式为 。
③用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液PH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体,下列说法不正确的是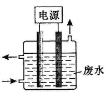
A.用石墨作阳极,铁作阴极
B.阳极的电极反应式为:Cl- + 2OH--2e-=ClO- + H2O
C.阴极的电极反应式为:2H2O + 2e-=H2↑ + 2OH-
D.除去CN-的反应:2CN-+ 5ClO- + 2H+ =N2↑ + 2CO2↑ + 5Cl-+H2O
(4)过碳酸钠(2Na2CO3·3H2O2)是一种集洗涤、漂白、杀菌于一体的氧系漂白剂,也可用于含氰废水的消毒。某兴趣小组制备过碳酸钠的实验方案和装置示意图如下: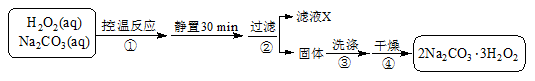
已知:2Na2CO3(aq)+ 3H2O2(aq) 2Na2CO3·3H2O2(s)ΔH<0,请回答下列问题:
2Na2CO3·3H2O2(s)ΔH<0,请回答下列问题:
①下列物质中,不会引起过碳酸钠发生氧化还原反应的有 。
A.FeCl3 B.CuSO4C.Na2SiO3 D.KCN
②准确称取0.2000g过碳酸钠于250mL锥形瓶中,加50 mL蒸馏水溶解,再加50 mL2.0 mol·L-1 H2SO4,用0.02000mol·L-1 KMnO4标准溶液滴定至终点时消耗30.00 mL,则产品中H2O2的质量分数为 。
[反应6KMnO4 + 5(2Na2CO3·3H2O2)+19H2SO4=3K2SO4 + 6MnSO4 +10Na2SO4 +10CO2↑ +15O2↑+34H2O]
电化学原理在防止金属腐蚀、能量转换、物质合成等方面应用广泛。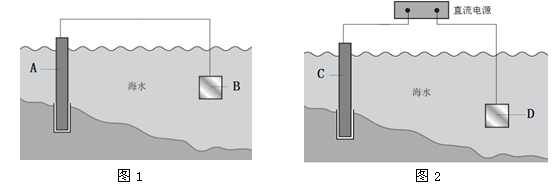
(1)图1中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择________(填字母序号)。
a.碳棒 b.锌板 c.铜板
用电化学原理解释材料B需定期拆换的原因:__________________________。
(2)图2中,钢闸门C做_____极。用氯化钠溶液模拟海水进行实验,D为石墨块,则D上的电极反应式为______________________,检测该电极反应产物的方法是_______________________。
(3)镁燃料电池在可移动电子设备电源和备用电源等方面应用前景广阔。图3为“镁—次氯酸盐”燃料电池原理示意图,电极为镁合金和铂合金。
①E为该燃料电池的极________(填“正”或“负”)。F电极上的电极反应式为___________。
②镁燃料电池负极容易发生自腐蚀产生氢气,使负极利用率降低,用化学用语解释其原因_______。
(1)下列有关说法正确的是_____________。
A.用pH试纸测得新制氯水的pH为4
B.碳酸钠和硫酸钡可按溶解、过滤、蒸发的操作顺序分离
C.除去C2H5OH中的CH3COOH,先加足量的氢氧化钠溶液,再分液
D.溶液中滴加盐酸酸化的BaCl2溶液出现白色沉淀,则该溶液中一定存在SO42-
E.将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中,检验气体中是否含有乙烯
F.用铂丝灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,没有K+
G.金属氧化物不一定是碱性氧化物,但碱性氧化物一定是金属氧化物;非金属氧化物不一定是酸性氧化物,酸性氧化物也不一定是非金属氧化物
H.在两个容积相同的容器中,一盛有HCl气体,另一个盛有H2和Cl2的混合气体,在同温同压下,两容器内的气体一定具有相同的原子数
I.实验室配制1mol/L盐酸250mL,需要的仪器只有:250mL容量瓶、胶头滴管、量筒和烧杯
J.在MH4Al(SO4)2(一种复盐)的溶液中加入Ba(OH)2溶液至沉淀的质量达到最大时:
Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
K.硝酸钡溶液中通入足量的SO2:2SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO↑+4H+
(2)ClO2的制备方法比较实用的有数十种,下列是几种常见的方法.
①方法一:2NaClO3+4HCl(浓)═2NaCl+Cl2↑+2ClO2↑+2H2O
对于该反应,下列说法中正确的是___________。
A.该反应中Cl2是氧化产物
B.该反应中NaCl、ClO2是还原产物
C.在反应中HCl既作氧化剂又具有酸的作用
D.1mol NaClO3参加反应时,有1mol电子发生转移
E.1mol NaClO3参加反应,理论上能得到33.6L气体
方法二:氯化钠电解法
该法工艺原理如图。
②其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。指出工艺中方框中物质为______(填化学式),理由为______________。
③将NCl3与NaClO2(亚氯酸钠)按物质的量之比1:6混合,在碱性溶液中恰好反应生成ClO2,试写出该反应的离子方程式____________。