(1)下列有关说法正确的是_____________。
A.用pH试纸测得新制氯水的pH为4
B.碳酸钠和硫酸钡可按溶解、过滤、蒸发的操作顺序分离
C.除去C2H5OH中的CH3COOH,先加足量的氢氧化钠溶液,再分液
D.溶液中滴加盐酸酸化的BaCl2溶液出现白色沉淀,则该溶液中一定存在SO42-
E.将乙醇与浓硫酸共热制得的气体通入酸性KMnO4溶液中,检验气体中是否含有乙烯
F.用铂丝灼烧白色粉末,火焰成黄色,证明原粉末中有Na+,没有K+
G.金属氧化物不一定是碱性氧化物,但碱性氧化物一定是金属氧化物;非金属氧化物不一定是酸性氧化物,酸性氧化物也不一定是非金属氧化物
H.在两个容积相同的容器中,一盛有HCl气体,另一个盛有H2和Cl2的混合气体,在同温同压下,两容器内的气体一定具有相同的原子数
I.实验室配制1mol/L盐酸250mL,需要的仪器只有:250mL容量瓶、胶头滴管、量筒和烧杯
J.在MH4Al(SO4)2(一种复盐)的溶液中加入Ba(OH)2溶液至沉淀的质量达到最大时:
Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O
K.硝酸钡溶液中通入足量的SO2:2SO2+2NO3-+3Ba2++2H2O=3BaSO4↓+2NO↑+4H+
(2)ClO2的制备方法比较实用的有数十种,下列是几种常见的方法.
①方法一:2NaClO3+4HCl(浓)═2NaCl+Cl2↑+2ClO2↑+2H2O
对于该反应,下列说法中正确的是___________。
A.该反应中Cl2是氧化产物
B.该反应中NaCl、ClO2是还原产物
C.在反应中HCl既作氧化剂又具有酸的作用
D.1mol NaClO3参加反应时,有1mol电子发生转移
E.1mol NaClO3参加反应,理论上能得到33.6L气体
方法二:氯化钠电解法
该法工艺原理如图。
②其过程是将食盐水在特定条件下电解得到的氯酸钠(NaClO3)与盐酸反应生成ClO2。指出工艺中方框中物质为______(填化学式),理由为______________。
③将NCl3与NaClO2(亚氯酸钠)按物质的量之比1:6混合,在碱性溶液中恰好反应生成ClO2,试写出该反应的离子方程式____________。
一定条件下,把3 mol N2和3 mol H2通入一个一定容积的密闭容器中,发生反应:
N2 (g)+3H2 (g) 2NH3(g)
2NH3(g)
达到平衡时,NH3的浓度为w mol·L-1,N2的转化率为m,则:
(1)H2的转化率________m(填“大于”“小于”“等于”或“无法确定”)。
(2)若在上述完全相同的容器中,维持温度不变,通入a mol NH3、b mol N2和c mol H2,要使达到平衡时,NH3的浓度仍为w mol·L-1。
若a=1,则b=________,c=________;b的取值范围为________。
(3)达到平衡时,H2和NH3均为1.5 mol,你认为是否可能?(填“可能”“不可能”或“无法确定”)。
某温度、压强下,向可变容积的密闭容器中充入了3 L A和2 L B,发生反应3A(g)+2B(g) xC(g)+yD(g),达到平衡时,C的体积分数为m%。若维持温度、压强不变,将0.6 L A、0.4 L B、4 L C、0.8 L D作为起始物质充入此密闭容器内,达到平衡时,C的体积分数仍为m%,则有x=______,y=______。
xC(g)+yD(g),达到平衡时,C的体积分数为m%。若维持温度、压强不变,将0.6 L A、0.4 L B、4 L C、0.8 L D作为起始物质充入此密闭容器内,达到平衡时,C的体积分数仍为m%,则有x=______,y=______。
在密闭容器中,充入一定量的N2和H2,在一定条件下合成氨,若以v(H2)、v(N2)分别表示消耗速率,v(NH3)表示分解速率,那么,该反应达到平衡前,用“>”“<”或“=”表示下列关系:
(1)v(H2)____________ (NH3)。
(NH3)。
(2)v(H2)____________3(N2)。
在120 ℃时分别进行如下四个反应:
| A.2H2S+O2====2H2O+2S↓ | B.2H2S+3O2====2H2O+2SO2 |
| C.C2H4+3O2=====2H2O+2CO2 | D.C4H8+6O2====4H2O+4CO2 |
(1)当反应在容积固定的容器内进行,反应前后气体密度(d)的气体总压强(p)分别符合关系式d前=d后和p前>p后的是____________;符合关系式d前=d后和p前=p后的是__________。(请填写反应的代号)
(2)若反应在压强恒定容积可变的容器内进行,反应前后气体密度(d)和气体体积(V)分别符合关系式d前>d后和V前<V后的是________,符合d前>d后和V前>V后的是_______。(请填写反应的代号)
如图:在一个容积固定的反应器中,有一可左右滑动的密封隔板,两侧分别进行如图所示的可逆反应。各物质的起始加入量如下:A、B和C均为4.0 mol,D为6.5 mol,F为2.0 mol,设E为x mol。当x在一定范围内变化时,均可以通过调节反应器的温度,使两侧反应都达到平衡,并且隔板恰好处于正中位置。请填写以下空白: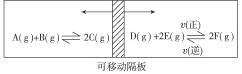
若x=4.5,则右侧反应在起始时向____________(填“正反应”或“逆反应”)方向进行。欲使起始反应维持向该方向进行,则x的最大取值应小于______________。
(2)若x分别为4.5和5.0,则在这两种情况下,当反应达平衡时,A的物质的量_________(填“相等”“不相等”或“不能确定”)。其理由是_______________。