(共11分)在下列物质转化关系中,反应的条件和部分产物已略去。
回答下列问题:
(1)若甲、乙是两种常见金属,且反应Ⅲ是工业制盐酸的反应。
①反应Ⅰ中甲在通常条件下和水剧烈反应,除丙外,还生成一种焰色反应为黄色的物质,则工业上生产甲的一般方法是 。
A.热分解法 B.热还原法 C.电解法
②反应Ⅱ中乙与H2O在高温下反应,除丙外,还生成一种有磁性的物质,则乙在周期表中的位置 ;反应Ⅱ的化学方程式是 。
(2)若甲、乙是离子化合物,且反应Ⅲ是工业上制漂白粉的反应。
①反应Ⅲ的离子方程式是 。
②若反应Ⅰ是气体实验室制备的反应,该气体分子为14电子结构。则反应Ⅰ的化学方程式是 。
③在饱和氯水中加块状石灰石,能制得较浓HClO溶液,同时放出一种气体。其反应的离子方程式是 ;写出HClO的结构式 。
硅是重要的半导体材料,构成了现代电子工业的基础。请回答下列问题:
(1)基态
原子中,电子占据的最高能层符号为,该能层具有的原子轨道数为、电子数为。
(2)硅主要以硅酸盐、等化合物的形式存在于地壳中。
(3)单质硅存在与金刚石结构类似的晶体,其中原子与原子之间以相结合,其晶胞中共有8个原子,其中在面心位置贡献个原子。
(4)单质硅可通过甲硅烷(
)分解反应来制备。工业上采用
和
在液氨介质中反应制得
,该反应的化学方程式为。
(5)碳和硅的有关化学键键能如下所示,简要分析和解释下列有关事实:
| 化学键 |
||||||
| 键能/( | 356 |
413 |
336 |
226 |
318 |
452 |
①硅与碳同族,也有系列氢化物,但硅烷在种类和数量上都远不如烷烃多,原因是。
②
的稳定性小于
,更易生成氧化物,原因是
(6)在硅酸盐中
4四面体(如下图(
))通过共用顶角氧离子可形成岛状、链状、层状、骨架网状四大类结构型式。图(
)为一种无限长单链结构的多硅酸根,其中
原子的杂化形式为
与
的原子数之比为化学式为。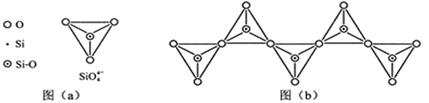
草酸(乙二酸)可作还原剂和沉淀剂,用于金属除锈、织物漂白和稀土生产。一种制备草酸(含2个结晶水)的工艺流程如下: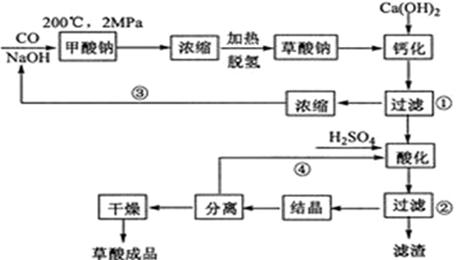
回答下列问题:
(1)
和
在一定条件下合成甲酸钠、甲酸钠加热脱氢的化学反应方程式分别为、。
(2)该制备工艺中有两次过滤操作,过滤操作①的滤液是,滤渣是;过滤操作②的滤液是和滤渣是。
(3)工艺过程中③和④的目的是。
(4)有人建议甲酸钠脱氢后直接用硫酸酸化制备草酸。该方案的缺点是产品不纯,其中含有的杂质主要是。
(5)结晶水合草酸成品的纯度用高锰酸钾法测定。称量草酸成品0.250g溶于水中,用0.0500
的酸性
溶液滴定,至粉红色不消褪,消耗
溶液15.00
,反应的离子方程式为;列式计算该成品的纯度。
二甲醚(
)是无色气体,可作为一种新型能源。由合成气(组成为
、
和少量的
)直接制备二甲醚,其中的主要过程包括以下四个反应:
甲醇合成反应:
(i)
+ 2
=
= -90.1
•
(ii) + 3 = + = -49.0 •
水煤气变换反应:
(iii)
+
=
+
= -41.1
•
二甲醚合成反应:
(iV)2
=
+
= -24.5
•
回答下列问题:
(1)
是合成气直接制备二甲醚反应催化剂的主要成分之一。工业上从铝土矿制备较高纯度
的主要工艺流程是(以化学方程式表示)。
(2)分析二甲醚合成反应(iV)对于
转化率的影响。
(3)由
和
直接制备二甲醚(另一产物为水蒸气)的热化学方程式为。根据化学反应原理,分析增加压强对直接制备二甲醚反应的影响。
(4)有研究者在催化剂(含
-
-
-
和
)、压强为5.0
的条件下,由
和
直接制备二甲醚,结果如下图所示。其中
转化率随温度升高而降低的原因是。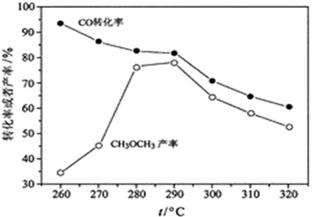
(5)二甲醚直接燃料电池具有启动快、效率高等优点,其能量密度等于甲醇直接燃料电池(5.93
•
•
)。若电解质为酸性,二甲醚直接燃料电池的负极反应为,一个二甲醚分子经过电化学氧化,可以产生个电子的能量;该电池的理论输出电压为1.20
,能量密度
=(列式计算。能量密度=电池输出电能/燃料质量,1
•
= 3.6×106
)。
锂离子电池的应用很广,其正极材料可再生利用。某锂离子电池正极材料有钴酸锂(
)、导电剂乙炔黑和铝箔等。充电时,该锂离子电池负极发生的反应为
。现欲利用以下工艺流程回收正极材料中的某些金属资源(部分条件未给出)。
回答下列问题:
(1)
中,
元素的化合价为。
(2)写出"正极碱浸"中发生反应的离子方程式。
(3)"酸浸"一般在80℃下进行,写出该步骤中发生的所有氧化还原反应的化学方程式;可用盐酸代替
和
的混合液,但缺点是。
(4)写出"沉钴"过程中发生反应的化学方程式。
(5)充放电过程中,发生
与
之间的转化,写出放电时电池反应方程式。
(6)上述工艺中,"放电处理"有利于锂在正极的回收,其原因是。在整个回收工艺中,可回收到的金属化合物有(填化学式)。
某市对大气进行监测,发现该市首要污染物为可吸入颗粒物
(直径小于等于2.5
的悬浮颗粒物)其主要来源为燃煤、机动车尾气等。因此,对
、
、
等进行研究具有重要意义。请回答下列问题:
(1)对
样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 |
||||||
| 浓度/ | 4×10-6 |
6×10-6 |
2×10-5 |
4×10-5 |
3×10-5 |
2×10-5 |
根据表中数据判断
的酸碱性为,试样的
值。
(2)为减少
的排放,常采取的措施有:
①将煤转化为清洁气体燃料。已知:
写出焦炭与水蒸气反应的热化学方程式;
②洗涤含
的烟气,以下物质可作洗涤剂的是;
a.
b.
c.
d.
(3)汽车尾气中
和
的生成及转化为:
①已知气缸中生成
的反应为:

若1
空气含有0.8
和0.2
,1300℃时在密闭容器内反应达到平衡。测得
为8×10-4
.计算该温度下的平衡常数K=;汽车启动后,气缸温度越高,单位时间内
排放量越大,原因是。
②汽车燃油不完全燃烧时产生
,有人设想按下列反应除去
:
已知该反应的
,简述该设想能否实现的依据。
③目前,在汽车尾气系统中装置催化转化器可减少
和
的污染,其化学反应方程式为。