一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,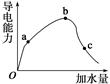
请回答:
(1)O点为什么不导电:_______________________________。
(2)a、b、c三点溶液的pH由小到大的顺序是______________。
(3)H+的物质的量最大的是________(填“a”、“b”或“c”)。
(4)若使c点溶液中的c(CH3COO-)增大,可以采取下列措施中的________(填序号)。
| A.加热 | B.加很稀的NaOH溶液 |
| C.加NaOH固体 | D.加水 |
E.加入锌粒
已知氯化铝的熔点为190℃(2.02×105Pa),但它在180℃和常压下即开始升华。
(1)氯化铝是晶体(填“离子”或“分子”)。
(2)在500℃,1.01×105Pa时,氯化铝的蒸气密度(换算成标准状况)为11.92g·L-1,且已知它的结构中还含有配位键,氯化铝的化学式为。
(3)设计一个更可靠的实验,证明氯化铝是离子晶体还是分子晶体,你的实验是。
(1)二氧化硅晶体中,每个硅原子周围有________个氧原子,每个氧原子周围有________个硅原子,硅氧原子个数比为________。
(2)石墨晶体结构如图所示,每一层由无数个正六边形构成。
平均每个正六边形所占有的碳原子数目为________、
平均每个正六边形所占有的共价键数目为________。
在金刚石的网状结构中,含有由共价键形成的碳原子环,其中最小的环上有(填数字)个碳原子,每个碳原子上的任意两个C—C键的夹角都是(填角度).
氯化钠属于 晶体,二氧化硅属于 晶体,NaCl和SiO2并不代表它们的 式,只能表示组成晶体的各种微粒的 。
榴石矿石可以看作CaO、Fe2O3、Al2O3、SiO2组成,由榴石矿石制取氯化钙和氧化铝的实验步骤如下:
(1)榴石矿加盐酸溶解后,溶液里除了Ca2+外,还含有的金属离子是________。
(2)对溶液Ⅰ进行操作时,控制溶液pH=9~10 (有关氢氧化物沉淀的pH见下表)NaOH不能过量,若NaOH过量可能会导致_________溶解,沉淀。
| 氢氧化物 |
Fe(OH)3 |
Al(OH)3 |
Ca(OH)2 |
| 开始沉淀pH |
1.5 |
3.3 |
12.0 |
(3)写出向沉淀物A中加入过量氢氧化钠溶液的离子方程式。
(4)①某同学在实验室中用图1装置制取CO2气体并通入溶液Ⅱ中,结果没有沉淀产生,可能的原是;为了能产生沉淀,该同学对图1装置进行了改进,改进的方法为。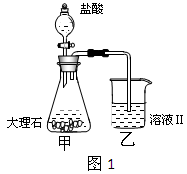
②若将二氧化碳气体通入澄清石灰水中,石灰水变浑浊,混合体系中除存在电离平衡、水解平衡外,还存在溶解平衡,用方程式表示该溶解平衡关系。