实验是进行化学研究的重要手段之一。请回答下列问题:
(1)下列实验操作,正确的是____________________(填写序号)。
a.称取氢氧化钠固体时,应将氢氧化钠固体直接放在左边托盘内,右边托盘放砝码
b.用纸槽往试管里装粉末状药品时,试管应先横放再直立
c.试管、烧杯、量筒、集气瓶都不能用酒精灯直接加热
d.配制硫酸溶液时,可先在量筒内加入一定体积的水,再在玻璃棒搅拌下慢慢加入浓硫酸
e.闻气体气味时,应取一瓶盛满气体的集气瓶,稍打开玻璃片,用手轻轻扇地在瓶口扇动,使极少量的气体飘进鼻孔,闻气味
(2)实验室需用1000mL 0.1 mol/L标准Na2CO3溶液,请回答下列问题
①在下图所示仪器中,配制上述溶液肯定不需要的是_________(填序号),除图中已有仪器外,配制上述溶液还需要的玻璃仪器有 _______ 。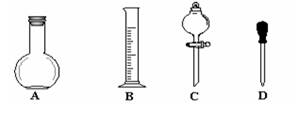
②在容量瓶的使用方法中,下列操作正确的是____________(填写序号)。
a.使用容量瓶前检验是否漏水
b.容量瓶用水洗净后,再用待配溶液洗涤
c.配制溶液时,若试样是液体,用量筒取样后用玻璃棒引流注入容量瓶中,然后加蒸馏水。
d.盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀。
③配制1000 mL 0.1 mol·L-1 Na2CO3溶液的实验步骤如下:
a.计算应称取碳酸钠固体的质量为________g。
b.称量碳酸钠固体。
c.将烧杯中的溶液注入容量瓶,并用少量蒸馏水洗涤烧杯内壁2~3次,洗涤液也注入容量瓶。
d.用适量的蒸馏水溶解称量好的碳酸钠固体,冷却。
e.盖好瓶塞,反复上下颠倒,摇匀。
f.继续向容量瓶中加蒸馏水至刻度线下1~2cm时,改用胶头滴管滴加蒸馏水至凹液面与刻度线相切。
上述步骤的正确操作顺序为_______________________(用序号表示)。
甲同学进行Fe2+还原性的实验,针对异常现象进行探究。
步骤一:制取FeCl2溶液。向0.1 mol•L-1 FeCl3溶液中加足量铁粉振荡,静置后取上层清液,测得pH<1。
步骤二:向2 mL FeCl2溶液中滴加2滴0.1 mol•L-1 KSCN溶液,无现象;再滴加5滴5% H2O2溶液(物质的量浓度约为1.5 mol•L-1、pH约为5),观察到溶液变红,大约10秒左右红色褪去,有气体生成(经检验为O2)。
(1)用离子方程式表示步骤二中溶液变红的原因:、。
(2)甲探究步骤二中溶液褪色的原因:
I.取褪色后溶液两份,一份滴加FeCl3溶液无现象;另一份滴加KSCN溶液出现红色;
II.取褪色后溶液,滴加盐酸和BaCl2溶液,产生白色沉淀。
III.向2 mL 0.1 mol•L-1 FeCl3溶液中滴加2滴0.1 mol•L-1 KSCN溶液,变红,通入O2,无明显变化。
实验I的说明;②实验III的目的是。
得出结论:溶液退色的原因是酸性条件下H2O2将SCN-氧化成SO42-。
(3)甲直接用FeCl2·4H2O配制①mol•L-1 的FeCl2溶液,重复步骤二中的操作,发现液体红色并未褪去。进一步探究其原因:
I.用激光笔分别照射红色液体和滴加了KSCN溶液的FeCl3溶液,前者有丁达尔效应,后者无。测所配FeCl2溶液的pH,约为3。由此,乙认为红色不褪去的可能原因是②。
II.查阅资料后推测,红色不褪去的原因还可能是pH较大时H2O2不能氧化SCN-。乙利用上述部分试剂,通过实验排除了这一可能。乙的实验操作及现象是:
| 步骤 |
试剂及操作 |
现象 |
| i |
③ |
生成白色沉淀 |
| ii |
向i所得溶液中滴加0.1 mol•L-1 FeCl3溶液 |
④ |
(15分)某兴趣小组利用下列实验装置进行探究实验。
根据要求回答下列问题:
(1)装置中长颈漏斗的作用有导气、。
(2)利用装置C可以证明S02具有漂白性,C中盛放的溶液是;若要证明其
漂白作用是可逆的,还需要的操作是。
(3)通过观察D中现象,即可证明S02具有氧化,D中盛放的溶液可以是。
a.NaCl溶液b.酸性KMn04c.FeCl3d.Na2S溶液
(4)研究小组发现B中有白色沉淀生成,若往B中加入过量稀盐酸,沉淀不溶解。沉淀物的化学式是。
(5)为进一步验证B中产生沉淀的原因,研究小组进行如下两次实验:
实验i:另取BaCl2溶液,加热煮沸,冷却后加入少量苯(起液封作用),然后再按照上述装置进行实验,结果发现B中沉淀量减少,但仍有轻微浑浊。
实验ii:用下图F装置代替上述实验中的A装置(其他装置不变),连接后往装置F中通入气体X一段时间,再加入70%H2S04溶液,结果B中没有出现浑浊。
①“实验i”中煮沸BaCl2溶液的目的是;
②气体X不可以是(填序号)。
a.C02b.03c.N2d.N02
③B中形成沉淀的原因是(用化学方程式表示):。
连二亚硫酸钠(Na2S2O4)又称保险粉,是印刷工业中重要的还原剂。某课题小组进行如下实验。
Ⅰ.查阅材料
(1)连二亚硫酸钠(Na2S2O4)是一种白色粉末,易溶于水,难溶于乙醇。
(2)2Na2S2O4+4HCl=4NaCl+S↓+3SO2↑+2H2O
Na2S2O3+2HCl=2NaCl+S↓+SO2↑+H2O
Ⅱ.制备方法
75℃时将甲酸钠和纯碱加入乙醇水溶液中,通入SO2进行反应,完成其反应方程式:
___HCOONa+___Na2CO3+_____ =___Na2S2O4+___CO2+___
=___Na2S2O4+___CO2+___
冷却至40-45℃,过滤,用______洗涤,干燥制得Na2S2O4
Ⅲ.Na2S2O4的性质
(1)Na2S2O4溶液在空气中易被氧化,课题小组测定0.050mol·L-1Na2S2O4溶液在空气中pH变化如右图:
0-t1段主要生成HSO3-,根据pH变化图,HSO3-的电离平衡水解平衡(填“<”或“>”),课题小组推测Na2S2O4溶液在空气中易被氧化,0-t1发生离子反应方程式为______________,t3时溶液中主要阴离子符号是_________。
(2)隔绝空气加热Na2S2O4固体完全分解得到固体产物Na2SO3、Na2S2O3和气体为__________(填化学式)。
请你设计实验验证产物有Na2S2O3存在,完成下表中内容:
(供选择的试剂:稀盐酸、稀硝酸、BaCl2溶液、KMnO4溶液)
| 实验步骤(不要求写出具体操作过程) |
预期的实验现象和结论 |
已知SO2可以用Fe(NO3)3溶液吸收,某学习小组据此按下图装置展开如下相关探究:取一定量的铜片于三颈烧瓶中,通入一段时间N2后再加入足量的浓硫酸,加热。装置A中有白雾(硫酸酸雾)生成,装置B中产生白色沉淀。
回答下列问题:
(1)装置A中用于添加浓硫酸的仪器名称为;检查图中连通装置A、B气密性的方法是。
(2)加入浓硫酸之前先通人N2一段时间,其目的是;排除装置A中白雾影响,可在装置A、B间增加洗气瓶C,则C中盛放的试剂是。若用氢氧化钠溶液处理尾气,则发生反应的离子方程式为。
(3)经过讨论,该小组对装置B中产生沉淀的原因,提出下列假设(不考虑各因素的叠加):
假设1:装置A中白雾进入装置B中参与了反应。
假设2:。
假设3:Fe(NO3)2溶液显酸性,在此酸性条件下NO3‾能氧化SO2。
(4)请你设计实验验证上述假设3,写出实验步骤、预期现象和结论。
| 实验步骤(简述操作过程) |
预期现象和结论 |
| ①测1.0mol•L‾1Fe(NO3)3溶液的pH; ② ③ ④ |
取碳酸钠和碳酸氢钠的混合粉末样品22.1g,将其加热到质量不再改变,冷却后称固体质量为15.9g,将得到的15.9g固体配成600mL溶液。则:原样品中碳酸氢钠的物质的量为mol;所配溶液中Na+的物质的量浓度为mol/L。