实验室用密度为1.18g/mL,质量分数为36.5%浓盐酸配制250mLO.lmol/L的稀盐酸溶液填空并请回答下列问题:
(1)使用容量瓶前必须进行的一步操作是______________________________;
(2)配制250mL0.lmol/L的盐稀酸溶液时,其正确的操作顺序是(字母表示,每个字母只能用一次)________________________________________;
| A.用30mL水洗涤烧杯2~3次,洗涤液均注入容量瓶,振荡 |
| B.用量筒准确量取所需浓盐酸体积__________mL,沿玻璃棒倒入烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其混合均匀 |
| C.将已冷却的盐酸沿玻璃棒注入mL的容量瓶中 |
| D.将容量瓶盖紧,振荡,摇匀 |
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度1~2cm处
(3)若出现如下情况,对所配溶液浓度将有何影响(填“偏高”、“偏低”或“无影响”)?若没有进行A操作浓度__________ ;若定容时俯视刻度线,浓度___________.
某课外活动小组探究镁与CO2、NO2的反应。
(1)实验发现点燃的镁条能在CO2气体中继续燃烧,产生黑、白两种固体,请用化学反应解释该现象 。
(2)该小组采用类比Mg与CO2反应的思路对Mg与NO2的反应进行预测:写出Mg与NO2反应的化学方程式 。
(3)设计实验验证猜测(用于连接玻璃管的乳胶管均内衬锡纸)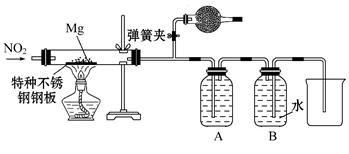
资料信息:2NO2+2NaOH====NaNO3+NaNO2+H2O。
①装置A中的试剂是 。
②干燥管和装置B的作用分别是 、
。
③实验开始时正确的操作步骤是 。
a.通入NO2
b.打开弹簧夹
c.点燃酒精灯
d.当硬质玻璃管充满红综色气体后,关闭弹簧夹
某学习小组进行浓硫酸对蔗糖的脱水实验,“在200 mL烧杯中放入20 g蔗糖(C12H22O11),加入适量水,搅拌均匀,然后再加入15 mL质量分数为98%的浓硫酸,迅速搅拌”进行如下探究。
(1)观察现象:蔗糖先变黄,再逐渐变黑,体积膨胀,形成疏松多孔的海绵状黑色物质,同时闻到刺激性气味。按压此黑色物质时,感觉较硬,放在水中呈漂浮状态。
同学们由上述现象推测出下列结论:①浓硫酸具有强氧化性;②浓硫酸具有吸水性;③浓硫酸具有脱水性;④浓硫酸具有酸性;⑤黑色物质具有强吸附性,其中依据不充分的是 (填序号)。
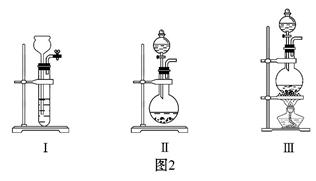
(2)为了验证蔗糖与浓硫酸反应生成的气态产物,同学们设计了如下装置:
试回答下列问题:
①图1的A中最好选用图2中的装置 (填编号)。
②图1的B装置所装试剂是 ;D装置中试剂的作用是 ;
E装置中发生的现象是 。
③图1的A装置中使蔗糖先变黑的化学反应方程式为
;
后体积膨胀的化学方程式为
。
④某学生进行实验时,发现D瓶品红不褪色,E装置中有气体逸出,F装置中酸性高锰酸钾溶液颜色变浅,推测F装置中酸性高锰酸钾溶液颜色变浅的原因
。
下面是某同学在学习硫元素时的学习方案,请完善该同学的学习方案。
(1)硫原子的结构:硫原子的核内质子数为16,它的原子结构示意图是 ,从结构可以知道硫元素是一种典型的非金属元素。
(2)硫单质的物理性质:硫是一种淡黄色的 体(填“气”“液”或“固”),主要存在于火山喷发口附近或地壳的岩层里,这是硫以游离态形式存在于自然界中。硫元素在自然界中也有以化合态形式存在的,如许多金属矿石是含硫化合物,如胆矾 (填化学式)。
(3)设计如下实验探究硫和含硫化合物的相互转化: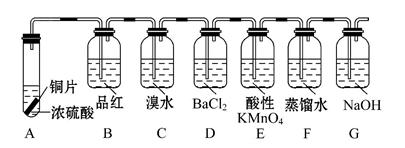
(Ⅰ)完成下列各个反应的化学方程式
①A中在加热时发生的反应
。
②C中的反应
。
(Ⅱ)记录观察到的实验现象
①B中品红溶液由红色变为 ,加热后又 ,(结论:可以根据该现象用品红溶液来证明SO2的存在与否)。
②D中没有观察到什么现象,在实验结束后往D中滴加H2O2后则可以看到 。
③E中溶液由紫红色变为无色,反应的离子方程式是
2Mn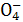 +5SO2+2H2O====2Mn2++5S
+5SO2+2H2O====2Mn2++5S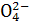 +4H+
+4H+
反应中SO2是 剂(填“氧化”或“还原”)。
(Ⅲ)G的作用是吸收尾气,写出反应的离子方程式:
。
二氧化硫通入氯化钡溶液中理论上不产生沉淀,而实际受到空气和溶液中氧气的影响很快便能观察到沉淀现象。为了避免产生沉淀,某化学小组设计了如下实验装置,实验操作步骤如下:
①气密性检查完好后,在装置A中的多孔隔板上放上锌粒,通过 注入稀硫酸、打开活塞,将产生的氢气导入到后续装置。
② 后关闭活塞,将装置D的导管插入烧杯中。
③通过装置B的 滴加浓硫酸,产生的气体进入到BaCl2溶液中,溶液保持澄清。
④打开活塞,将产生的氢气导入后续装置一段时间。
⑤将盛有BaCl2溶液的试管从装置中取出,拔去橡皮塞用胶头滴管伸入到苯层下方滴加双氧水,随即出现白色浑浊,滴加稀盐酸并振荡,白色浑浊不消失。
⑥拆卸装置,清洗仪器,处理剩余药品。
请回答下列问题:
(1)实验步骤①和③的空白处使用的仪器分别为 、 ;
(2)装置C中苯的作用是 ;
(3)实验步骤②的操作为 ;
(4)实验步骤④的目的是 ;
(5)写出实验步骤⑤试管中发生反应的化学方程式
、 ;
(6)为了避免产生沉淀,你认为还应采取哪些措施,请举一例 。
硫酸工业尾气中二氧化硫含量超过0.05%(体积分数)时需经处理后才能排放。某校兴趣小组欲测定硫酸工业尾气中二氧化硫含量,采用以下方案:
甲方案:如图所示,图中气体流量计B用于准确测量通过尾气的体积。将尾气通入一定体积已知浓度的碘水中测定二氧化硫的含量。当洗气瓶C中溶液蓝色消失时,立即关闭活塞A。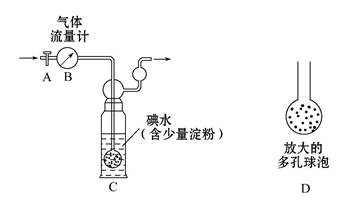
(1)洗气瓶C中导管末端连接一个多孔球泡D,可以提高实验准确度,其理由是
。
(2)洗气瓶C中的溶液可以用其他试剂替代,请你举出一种: 。
(3)洗气瓶C溶液蓝色消失后,没有及时关闭活塞A,测得的SO2含量 (填“偏高”“偏低”或“无影响”)。
乙方案:实验步骤如以下流程图所示: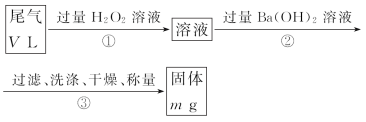
(4)写出步骤②中反应的化学方程式 。
(5)步骤③中洗涤沉淀的方法是 。
(6)通过的尾气体积为VL(已换算成标准状况)时,该尾气中二氧化硫含量(体积分数)为 (用含有V、m的代数式表示)。
丙方案:将乙方案中步骤①省略,直接将尾气通入过量Ba(OH)2溶液,其余步骤与乙方案相同。
(7)你认为丙方案是否合理,说明理由:
。