(14分)氢能以其洁净、高效、高热值、环境友好等特点成为最有前途的新能源,制氢和储氢的方法有很多。
(1)下图所示电化学装置工作时均与H2有关。
①图A所示装置可用于电解K2MnO4制KMnO4,通电一段时间后阴极附近溶液的pH将会 (填“增大”、“减小”或“不变”) 。
②图B所示装置为吸附了氢气的纳米碳管等材料制作的二次电池的原理,
开关连接用电器时,镍电极发生 (填“氧化”或“还原”)反应;开关连接充电器时,阳极的电极反应为 。
(2)热化学循环法制氢。已知:
①2Br2(g)+2CaO(s) == 2CaBr2(s)+O2(g) △H= —146kJ·mol—1
②3FeBr2(s)+4H2O(g) == Fe3O4(s)+6HBr(g)+H2(g) △H= +384kJ·mol—1
③CaBr2(s)+H2O(g) == CaO(s)+2HBr(g) △H= +212kJ·mol—1
④Fe3O4(s)+8HBr(g) == Br2(g)+3FeBr2(s)+4H2O(g) △H= —274kJ·mol—1
则2H2O(g) == 2H2(g)+O2(g)的△H= kJ·mol—1。
(3)光电化学分解制氢,原理如图所示,钛酸锶光电极的电极反应为4OH–– 4e–===O2+2H2O,则铂电极的电极反应为 。
(4)生物质制氢,若将生物质气化炉中出来的气体[主要有CH4、CO2、H2O(g)、CO及H2]在1.01×105Pa下进入转换炉,改变温度条件,各成分的体积组成关系如下图所示。下列有关图像的解读正确的是 。
| A.利用CH4与H2O(g)及CO2转化为合成气CO和H2理论上是可行的 |
| B.CH4(g)+CO2(g)→2CO(g)+2H2(g)和CH4(g)+H2O(g) → CO(g)+3H2(g),都是放热反应 |
| C.CH4与CO2及H2O(g)转化为合成气CO和H2的适宜温度约为900℃ |
| D.图像中曲线的交点处表示反应达到平衡 |
(5)LiBH4具有非常高的储氢能力,分解时生成氢化锂和两种单质,试写出该分解反应的化学方程式 。
某实验小组依据反应 设计如图1原电池,探究pH对AsO4 氧化性的影响。测得电压与pH的关系如图2。下列有关叙述不正确的是( )
设计如图1原电池,探究pH对AsO4 氧化性的影响。测得电压与pH的关系如图2。下列有关叙述不正确的是( )
| A.调节pH可以改变反应的方向 |
| B.pH=0.68时,反应处于平衡状态 |
| C.pH=5时, 负极电极反应式为2I--2e -= I2 |
| D.pH>0.68时,氧化性I2>AsO43- |
氧化剂和还原剂在生产生活中广泛使用。
(1)高锰酸钾和氢溴酸溶液可以发生如下反应:
2KMnO4+ 16HBr = 5Br2+ 2MnBr2+ 2KBr+ 8H2O
①其中还原剂为 ,还原产物为
②若有0.8 mol还原剂被氧化,则转移电子的物质的量是
(2)双氧水H2O2可作为矿业废液消毒剂,可以消除采矿业废液中的氰化物(如KCN,其中N为﹣3价),化学方程式为:KCN+H2O2+H2O═KHCO3+A↑(已配平)
①生成物A的化学式为
②用双线桥法表示该反应中电子转移的方向和数目:
(3)古老但仍然是最有用的制备联氨(N2H4)溶液的方法如下:
NaClO+ NH3·H2O 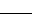 N2H4 + NaCl+ H2O
N2H4 + NaCl+ H2O
①请配平上述化学方程式
②NH3·H2O在上述反应中显示出来的性质是
| A.氧化性 | B.还原性 | C.酸性 | D.碱性 |
(4)人体内所含铁元素以Fe2+和Fe3+的形式存在市场出售的某种麦片中含有微量的颗粒细小的还原铁粉,这些铁粉在人体胃酸的作用下转化成亚铁盐,此反应的离子方程式为 ,但Fe2+在酸性条件下很容易被空气中的氧气氧化,写出该反应的离子方程式
实验室现有一瓶2%氢氧化钠溶液(ρ="1.22" g/mL)。
(1)该氢氧化钠溶液的物质的量浓度为
(2)由于实验需要,现还需该浓度氢氧化钠溶液230 mL,需要临时配制。
①应选择 mL的容量瓶,容量瓶使用时第一步操作是
②需要的玻璃仪器除了容量瓶、量筒外,还有
③用托盘天平称取 g NaOH
④经过测定,某同学配制的氢氧化钠浓度偏高,则可能的原因是
| A.容量瓶中残存少量蒸馏水 |
| B.称取NaOH固体时,直接在纸片上称取 |
| C.溶解的NaOH溶液未冷却到室温,就转移到容量瓶中并定容 |
| D.洗涤烧杯内壁后将洗涤液弃去 |
E.定容时,俯视容量瓶刻度线
F.定容、摇匀后发现溶液的凹液面低于刻度线
(3)取该氢氧化钠溶液20 mL,加入0.5 mol/L硫酸溶液10 mL,然后把混合溶液稀释至100 mL,则稀释后的溶液中OH﹣的浓度为
A、B、C、D为四种可溶性的盐,它们包含的阳离子和阴离子分别为Ba2+、Ag+、Na+、Cu2+和NO3﹣、SO42﹣、Cl﹣、CO32﹣(离子在物质中不能重复出现)。
①若把四种盐分别溶于盛有蒸馏水的四支试管中,只有C盐的溶液呈蓝色;
②若向①的四支试管中分别加入盐酸,B盐的溶液有沉淀生成,D盐的溶液有无色无味的气体逸出.根据①②实验事实可推断它们的化学式为:
(1)A B
(2)写出盐酸与D反应的离子方程式:
(3)将含相同物质的量A、B、C的溶液混合后,写出溶液中存在的离子及物质的量之比 ;在此溶液中加入锌粒,写出发生反应的离子方程式
(4)C溶液中阴离子的检验方法:
现有下列九种物质:①HCl气体 ②Cu ③C2H5OH ④CO2 ⑤CuSO4 ·5H2O ⑥FeCl3固体 ⑦碘水 ⑧Ba(OH)2溶液 ⑨熔融Al2(SO4)3
(1)属于电解质的是 ;属于非电解质的是
(2)⑤在水中的电离方程式为
(3)171g ⑨溶于水配成500 mL溶液,SO42﹣的物质的量浓度为
(4)用洁净的烧杯取25 mL蒸馏水,加热至沸腾,向烧杯中逐滴加入上述五种物质中的某一物质的饱和溶液,加热得红褐色胶体,该反应的离子方程式为
(5)写出⑤的溶液和⑧反应的离子方程式
(6)要从⑦中提取纯净的碘,需要采取的操作有 、 、 (填写操作名称)