下列叙述中正确的是
(1)纯铁比碳素钢易生锈
(2)用氨水除去试管上的银镜
(3)硅是制作光导纤维和制造太阳能电池的主要原料
(4)可用稀盐酸、碳酸钠溶液、硅酸钠溶液设计实验来验证元素的非金属性
(5)催化剂只能改变反应的活化能,不能改变反应的热效应
(6)用氢氟酸雕刻玻璃是利用氢氟酸能与二氧化硅反应的性质
(7)同主族元素的简单阴离子还原性越强,水解程度越大
(8) 在工业上用于制作耐高温材料,也用于电解法治炼铝
在工业上用于制作耐高温材料,也用于电解法治炼铝
(9)丁达尔效应可用于区别溶液与胶体,云、雾均能产生丁达尔效应
(10)明矾可用于水的消毒、杀菌;碳酸钡可用于钡餐透视
| A.(1)(4)(6)(7) | B.(4)(6)(9)(10) |
| C.(3)(5)(6)(8) | D.(5)(6)(8)(9) |
“类推”的思维方式在化学学习与研究中经常采用。下列类推思维中正确的是
| A.NaOH饱和溶液导电能力强,则Ca(OH)2饱和溶液导电能力也强 |
| B.CaC2能水解:CaC2+2H2O→Ca(OH)2+HC≡CH,则Mg2C2也能水解:Mg2C2+4H2O→2Mg(OH)2+CH3—C≡CH |
| C.加热时Cu与O2反应生成CuO,则加热时Cu与S反应生成CuS |
| D.BaCl2溶液中通入SO2无沉淀产生,则Ba(NO3)2溶液中通入SO2也无沉淀产生 |
下列实验过程中产生的现象与图中曲线变化相对应的是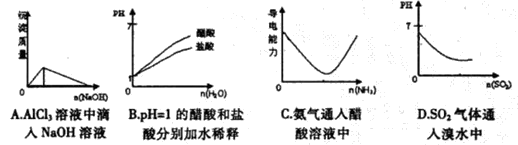
观察下列几个装置示意图,有关叙述正确的是
| A.装置①中阳极上析出红色固体 |
| B.装置②中铜片应与电源负极相连 |
| C.装置③中外电路电流方向:b极 →a极 |
| D.装置④中阴极反应:2 Cl--2e-= Cl2 |
下列实验操作及现象与实验结论一致的是
| 选项 |
实验操作及现象 |
实验结论 |
| A |
向某溶液中加入盐酸酸化的BaCl2溶液,生成白色沉淀 |
该溶液中不一定含有 |
| B |
光洁的铁钉放在冷的浓硫酸中,无明显现象 |
铁钉与冷的浓硫酸不反应 |
| C |
将少量的溴水分别滴入FeCl2溶液、NaI溶液中,再分别滴加CCl4振荡静置,下层分别呈无色和紫红色 |
氧化性:Br2> Fe3+>I2 |
| D |
向浓度均为0.1mol•L-1的KCl、KI混合溶液中滴加AgNO3 |
Ksp(AgCl)< Ksp (AgI) |
下列叙述正确的是
| A.浓度均为0.1mol•L—1的CH3COOH和CH3COONa溶液等体积混合所得的溶液中: c(CH3COOH)+c(CH3COO—)=0.2mol•L-1 |
| B.0.1mol•L-1NaHCO3溶液中:c(Na+)=c(HCO3-)+c(H2CO3)+2(CO32-) |
| C.0.2mol•L-1HCl溶液与等体积0.1mol•L-1NaOH溶液混合后,溶液的pH=1 |
| D.0.1mol•L-1氨水中滴入0.1mol•L-1盐酸至溶液呈中性时,混合溶液中:c(NH4+)=c(Cl—) |