根据表中信息,判断下列叙述中正确的是
| A.表中①组的反应可能有一种或两种元素被氧化 |
| B.氧化性强弱的比较: KClO3>Fe3+>Cl2>Br2 |
| C.表中②组反应的还原产物是KCl,电子转移数目是6e- |
| D.表中③组反应的离子方程式为:2MnO4-+ 3H2O2 + 6H+=2Mn2+ + 4O2↑+ 6H2O |
一定条件下,PbO2与Cr3+反应,产物是Cr2O72-和Pb2+,则生成1 mol Cr2O72-反应所需PbO2的物质的量为
| A.3.0 mol | B.1.5 mol | C.1.0 mol | D.0.75 mol |
黑火药是由硫黄粉、硝酸钾和木炭按一定比例混合而成的,爆炸时的反应是:
S+2KNO3+3C = K2S+N2↑+3CO2↑,该反应的还原剂是
| A.C | B.C和S | C.KNO3 | D.S和KNO3 |
下列各组离子一定能大量共存的是
| A.在无色溶液中:NH4+、Fe2+、SO42-、CO32- |
| B.在含大量Ba2+的溶液中:Cu2+、Na+、Cl-、OH- |
| C.在强酸性溶液中:K+、Fe2+、Cl-、CH3COO- |
| D.在强碱溶液中:Na+、K+、Cl-、SO32- |
除去下列物质中的少量杂质(括号内的物质为杂质),加入试剂或方法不正确的是
| A.NaCl溶液(BaCl2):加入足量Na2CO3溶液,过滤,再向滤液中加适量盐酸并加热 |
| B.KNO3溶液(AgNO3):加入足量KCl溶液,过滤 |
| C.NaCl固体(Na2CO3):加适量稀盐酸,加热蒸发 |
| D.CO2(HCl):将混合气体通过NaHCO3饱和溶液 |
现有四组分散系:①汽油和水形成的乳浊液;②含有泥沙的食盐水;③溶有碘(I2)的碘化钾溶液;④乙二醇和丙三醇混合溶液(乙二醇和丙三醇的部分物理性质见下表)。
| 物质 |
熔点/℃ |
沸点/℃ |
密度/g·cm-3 |
溶解性 |
| 乙二醇 |
-11.5 |
198 |
1.11 |
易溶于水和乙醇 |
| 丙三醇 |
17.9 |
290 |
1.26 |
能跟水、酒精以任意比互溶 |
请用下图所示的仪器分离以上各混合液,仪器和方法不能对应的是
⑴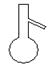 ⑵
⑵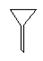 ⑶
⑶ ⑷
⑷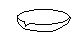
A.①-⑶-分液B.②-⑵-过滤
C.③-⑵-萃取D.④-⑴-蒸馏