(10分)“低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO
和H2为主的合成气,合成气有广泛应用。试回答下列问题:
(1)高炉炼铁基本反应为:FeO(s)+CO(g) Fe(s)+CO2(g) ΔH>0。已知在1 100 ℃时,该反应的化学平衡常数K=0.263。
Fe(s)+CO2(g) ΔH>0。已知在1 100 ℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值 (填“增大”、“减小”或“不变”);
②1100 ℃时测得高炉中,c(CO2)="0.025" mol·L-1,c(CO)="0.1" mol·L-1,则在这种情况下,该反应向 进行(填“左”或“右”),判断依据是 。
(2)目前工业上也可用CO2来生产燃料甲醇,有关反应为:CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,现向体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1,现向体积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。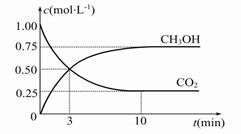
①从反应开始到平衡,氢气的平均反应速率v(H2)= 。
②反应达到平衡后,下列措施能使[CH3OH]∕[CO2]增大的是 (填符号)。
| A.升高温度 |
| B.再充入H2 |
| C.再充入CO2 |
| D.将H2O(g)从体系中分离 |
E.充入He(g)
下图为番茄电池,下列说法正确的是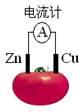
| A.一段时间后,锌片质量会变小 | B.铜电极附近会出现蓝色 |
| C.电子由铜通过导线流向锌 | D.锌电极是该电池的正极 |
据报道,氢燃料电池公交汽车已经驶上北京街头。下列说法正确的是
| A.电解水制取氢气是理想而经济的制氢方法 |
| B.发展氢燃料电池汽车不需要安全高效的储氢技术 |
| C.氢燃料电池把氢气和氧气燃烧放出的热能转化为电能 |
| D.氢燃料电池汽车的使用可以有效减少城市空气污染 |
在2A(g)+ B(s) =" 3C(g)+" 4D(g)反应中,表示该反应速率最快的数据是
| A.υA = 0.6mol/(L·s) | B.υB = 0.3mol/(L·s) |
| C.υC =" 0.8mol/(L·s)" | D.υD = 1.0mol/(L·s) |
关于可逆反应达到平衡状态的说法错误的是
| A.达平衡时正、逆反应速率相等 | B.是动态平衡 |
| C.各组分的含量不随时间而变化 | D.外界条件不能改变平衡 |
下列各项比较中错误的是
| A.原子半径:Li<Na<K | B.酸性: H2SiO3 < H2CO3 < HNO3 < HClO4 |
| C.稳定性: SiH4 > H2S> HF | D.碱性: NaOH > Mg(OH)2 > Be (OH)2 |