下列叙述中不正确的是
| A.电解池的阳极上发生氧化反应,阴极上发生还原反应 |
| B.不能自发进行的氧化还原反应可通过电解的原理实现 |
| C.电镀时,电镀池里的阳极材料发生氧化反应 |
| D.电解饱和食盐水时,阳极得到氢氧化钠溶液和氢气 |
甲、乙两溶液中,分别含有大量的Cu2+、K+、H+、Cl-、CO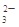 、OH-6种离子中的3种,已知甲溶液呈蓝色,则乙溶液中大量存在的离子是
、OH-6种离子中的3种,已知甲溶液呈蓝色,则乙溶液中大量存在的离子是
A.K+、OH-、CO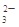 |
| B.Cu2+、H+、Cl- |
| C.K+、H+、Cl- |
D.CO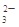 、OH-、Cl- 、OH-、Cl- |
从海带中提取碘的实验过程中,涉及下列操作,其中正确的是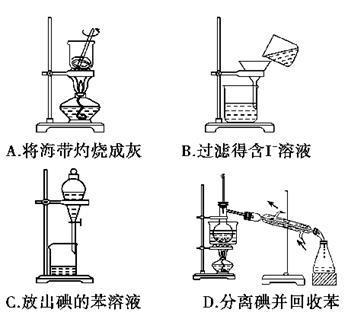
下列各反应中,氧化反应与还原反应在同种元素中进行的是
| A.Cl2+2NaOH===NaCl+NaClO+H2O |
B.2KClO3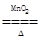 2KCl+3O2↑ 2KCl+3O2↑ |
C.2KMnO4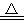 K2MnO4+MnO2+O2↑ K2MnO4+MnO2+O2↑ |
D.2H2O 2H2↑+O2↑ 2H2↑+O2↑ |
下列叙述中正确的是
| A.将SO2通入酸性高锰酸钾溶液中,溶液褪色,不能说明SO2具有漂白性 |
| B.浓盐酸和浓硫酸暴露在空气中浓度都会降低,其原因相同 |
| C.向某无色溶液中滴加氯化钡溶液,产生白色沉淀,再加入稀盐酸后该沉淀不溶解,说明原溶液中一定含有SO42- |
| D.土壤中的闪锌矿(ZnS)遇到硫酸铜溶液转化为铜蓝(CuS),说明CuS很稳定,不具有还原性 |
NA为阿伏伽德罗常数,下列说法正确的是
| A.18gD2O和18gH2O中含有的质子数均为10NA |
| B.高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA |
| C.欲配制1.00L 1.00mol·L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中 |
| D.过氧化钠与水反应时,生成0.1mol氧气转移的电子数为0.2NA |