某恒容容器内发生的可逆反应的化学平衡常数表达式为: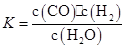 。能判断该反应一定达到化学平衡状态的依据是( )
。能判断该反应一定达到化学平衡状态的依据是( )
①容器中气体的平均相对分子质量不随时间而变化
②v正(H2O)=v逆(H2)
③容器中气体的密度不随时间而变化
④容器中气体总质量不随时间而变化
⑤消耗n mol H2的同时消耗n mol CO
| A.①②③ | B.①②③④ | C.② | D.①④⑤ |
溶液中,反应A+2B C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol/L、c(B )="0.200" mol/L及c(C )="0" mol/L。反应物A的浓度随时间的变化如图所示。
C分别在三种不同实验条件下进行,它们的起始浓度均为c(A)="0.100" mol/L、c(B )="0.200" mol/L及c(C )="0" mol/L。反应物A的浓度随时间的变化如图所示。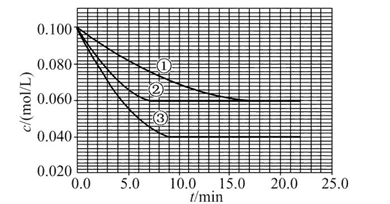
请回答下列问题:
(1)与①比较,②和③分别仅改变一种反应条件。所改变的条件和判断的理由是:②;③。
(2)实验②平衡时B的转化率为;实验③平衡时C的浓度为。
(3)该反应的ΔH0,其判断理由是。
(4)该反应进行到4.0 min时的平均反应速率:实验②:v(B)=。
硫-碘循环分解水制氢主要涉及下列反应:
Ⅰ.SO2+2H2O+I2=H2SO4+2HI
Ⅱ.2HI H2↑+I2
H2↑+I2
Ⅲ.2H2SO4=2SO2+O2↑+2H2O
(1)分析上述反应,下列判断正确的是。
a.反应Ⅲ易在常温下进行
b.反应Ⅰ中SO2氧化性比HI强
c.循环过程中需补充H2O
d.循环过程中产生1 mol O2的同时产生1 mol H2
(2)一定温度下,向1 L密闭容器中加入1 mol HI(g),发生反应Ⅱ,H2的物质的量随时间的变化如图所示。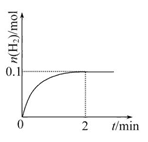
①0~2 min内的平均反应速率v(HI)=。
②相同温度下,若开始加入HI(g)的物质的量是原来的2倍,则是原来的2倍。
a.HI的平衡浓度
b.达到平衡的时间
c.平衡时H2的体积分数
(3)实验室用Zn和稀硫酸制取H2,若加入少量下列固体试剂中的,产生H2的速率将增大。
a.NaNO3b.CuSO4c.Na2SO4d.NaHSO3
下列框图中A、F、G、H都是芳香族化合物。A的相对分子质量不超过200,完全燃烧只生成CO2和H2O;A中氧元素的质量分数为8/30。
又已知:① E能发生银镜反应,G不能发生银镜反应;②F与FeCl3溶液不显紫色。
回答下列问题:
(1)下列叙述正确的是。
(A)A的分子式是C10H14O3
(B)A能发生氧化、还原、取代、消去等反应
(C)1molA最多能与3mol H2发生加成反应
(D)A能与NaHCO3溶液反应放出CO2
(2)F分子中含有的官能团的名称是:。
(3)由F转化成H的反应类型属于。
(4)写出B+D→E的化学方程式:。
(5)写出F→G的化学方程式:。
(6)H的同分异构体甚多。请写出符合下列条件的同分异构体的结构简式(任写三种):
①苯环上只有一个链状取代基;②能够与NaOH溶液反应。。
大气中的部分碘源于O3对海水中Iˉ的氧化。将O3持续通入NaI酸性溶液溶液中进行模拟研究。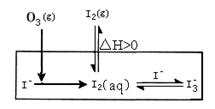
(1)O3将Iˉ氧化成I2的过程可发生如下反应:
①Iˉ(aq)+ O3(g)= IOˉ(aq) +O2(g)△H1
②IOˉ(aq)+H+(aq)  HOI(aq) △H2
HOI(aq) △H2
③HOI(aq) + Iˉ(aq) + H+(aq) I2(aq) + H2O(l)△H3
I2(aq) + H2O(l)△H3
④O3(g)+2Iˉ(aq)+2H+(aq)= I2(aq) + O2(g)+ H2O(l)△H4
则△H3与△H1、△H2、△H4之间的关系是:△H3=。
(2)在溶液中存在化学平衡: I2(aq) + Iˉ(aq)  I3ˉ(aq)其平衡常数表达式为。在反应的整个过程中I3ˉ物质的量浓度变化情况是。
I3ˉ(aq)其平衡常数表达式为。在反应的整个过程中I3ˉ物质的量浓度变化情况是。
(3)为探究温度对I2(aq) + Iˉ(aq) I3ˉ(aq)△H5反应的影响。在某温度T1下,将一定量的0.2 mol·L-1NaI酸性溶液置于密闭容器中,并充入一定量的O3(g)(O3气体不足,不考虑生成物O2与 Iˉ反应),在t时刻,测得容器中I2(g)的浓度。然后分别在温度为T2、T3、T4、T5下,保持其它初始实验条件不变,重复上述实验,经过相同时间测得I2(g)浓度,得到趋势图(见图一)。则:
I3ˉ(aq)△H5反应的影响。在某温度T1下,将一定量的0.2 mol·L-1NaI酸性溶液置于密闭容器中,并充入一定量的O3(g)(O3气体不足,不考虑生成物O2与 Iˉ反应),在t时刻,测得容器中I2(g)的浓度。然后分别在温度为T2、T3、T4、T5下,保持其它初始实验条件不变,重复上述实验,经过相同时间测得I2(g)浓度,得到趋势图(见图一)。则: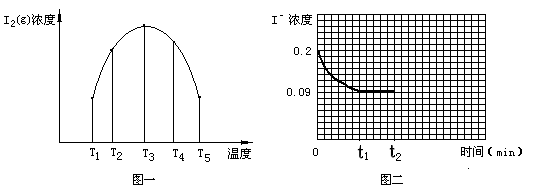
①若在T3时,容器中无O3, T4~T5温度区间容器内I2(g)浓度呈现如图一所示的变化趋势,则△H50(填>、=或<);该条件下在温度为T4时,溶液中Iˉ浓度随时间变化的趋势曲线如图二所示。在t2时,将该反应体系温度上升到T5,并维持该温度。请在图2中画出t2时刻后溶液中 Iˉ浓度变化总趋势曲线。
②若在T3时,容器中还有O3,则T1~T2温度区间容器内I2(g)浓度呈现如图一所示的变化趋势,其可能的原因是。(任写一点)
(4)利用反应④和图2的信息,计算0-t1时间段内用I2(aq)表示的化学反应速率。