下列各组微粒的空间构型相同的是
①NH3和H2O ②NH4+和H3O+③NH3和H3O+④O3和SO2⑤CO2和C2H2⑥SiO44-和SO42-
| A.全部 | B.除①④⑥以外 | C.③④⑤⑥ | D.②⑤⑥ |
下列说法正确的是( )
| A.离子化合物中只能含有离子键 |
| B.共价化合物中可能含有离子键 |
| C.化学键存在于分子之间 |
| D.化学反应的过程,本质上是旧化学键断裂和新化学键形成的过程 |
某元素原子的原子核外有三个电子层,最外层电子数是4,该原子核内的质子数是( )
| A.14 | B.15 | C.16 | D.17 |
下列各组粒子中属于同位素的是( )
| A.16O和18O | B.H2O和D2O | C.H2和D2 | D.24Mg和24Na |
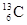 -NMR(核磁共振)可用于含碳化合物的结构分析,
-NMR(核磁共振)可用于含碳化合物的结构分析,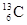 表示的是( )
表示的是( )
| A.核外有13个电 子,其中6个能参与成键 |
| B.核内有6个质子,核外有7个电子 |
| C.质量数是13,原子序数是6,核内有7个质子 |
| D.质量数是13,原子序数是6,核内有7个中子 |
下列溶液中有关物质的量浓度关系正确的是()
| A. |
=2的 溶液与 =12的 溶液任意比混合: ( ) + ( )> ( ) + ( ) |
| B. |
相等的 、 和 三种溶液: ( )< ( )< ( ) |
| C. |
物质的量浓度相等 和 溶液等体积混合: ( )+ ( )= ( ) + ( ) |
| D. |
0.1 -1的 溶液,其 =4: ( )> ( )> ( )> ( ) |