在一容积为2 L的密闭容器中,加入0.2 mol的N2和0.6 mol的H2,在一定条件下发生反应:N2(g)+3H2(g) 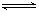 2NH3(g) ΔH<0反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题:
2NH3(g) ΔH<0反应中NH3的物质的量浓度的变化情况如下图所示,请回答下列问题: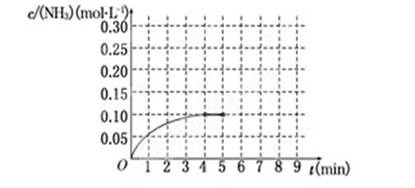
(1)根据上图,计算从反应开始到平衡时,平衡反应速率v(NH3)为__________.
(2)该反应达到平衡时H2的转化率为________.
(3)反应达到平衡后,第5分钟末,保持其它条件不变,若改变反应温度,则NH3的物质的量浓度不可能为________.(填序号)
a.0.20 mol·L-1 b.0.12 mol·L-1
c.0.10 mol·L-1 d.0.08 mol·L-1
(4)请写出该反应的平衡常数表达式___ ______,若该反应在298K、398K时的化学平衡常数分别为K1、K2,则K1 K2(填“>”“="”" 或 “<” )。
(5)在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时NH3的浓度约为0.25mol·L-1),请在上图中画出第5分钟末到此平衡时NH3浓度的变化曲线.
现用质量分数为98%、密度为1.84 g·cm-3的浓H2SO4来配制500 mL、0.2 mol·L-1的稀H2SO4。可供选择的仪器有:
①玻璃棒 ②烧瓶 ③烧杯 ④胶头滴管 ⑤量筒 ⑥容量瓶 ⑦托盘天平 ⑧药匙。
请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有_____________________ (填代号)。
(2)经计算,需浓H2SO4的体积为。
(3)在配制过程中,其他操作都准确,下列操作中:能引起误差偏高的有(填代号)。
①洗涤量取浓H2SO4后的量筒,并将洗涤液转移到容量瓶中;
②未等稀释后的H2SO4溶液冷却至室温就转移到容量瓶中;
③定容时,加蒸馏水超过标线,又用胶头滴管吸出
④转移前,容量瓶中含有少量蒸馏水
⑤定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑥定容时,俯视标线
填空题
(1)下图所示是分离混合物时常用的仪器,回答下列问题: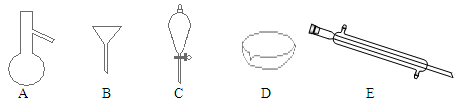
①写出仪器A、C、E的名称、、
②分离以下混合物应该主要选用上述什么仪器?(填字母符号)
A.粗盐和泥沙:B.花生油和水:
(2)写出下列物质溶于水时的电离方程式:
①Fe2(SO4)3
②NaHSO4
③KMnO4
(10分)下图是一种药物分子合成的部分路线图(反应条件已经略去):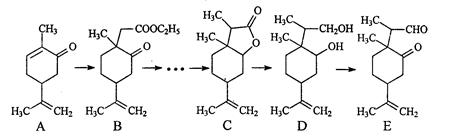
已知①LiBH4可将醛、酮、酯类还原成醇,但不能还原羧酸、羧酸盐、碳碳双键,遇酸分解。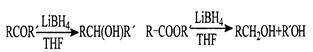
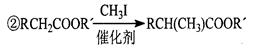
(1)写出一种满足下列条件的A的同分异构体的结构简式为
①属于芳香族化合物;②能使FeCl3溶液显色;③分子中有4种不同化学环境的氢原子。
(2)有机物E分子中含氧官能团名称为。
(3)C用LiBH4还原可以得到D。C→D不直接用氢气(镍作催化剂)还原的原因是。
(4)检验D是否完全转化为E的实验方法是(用化学方程式表示)
(5)请写出B→C的合成路线图(CH3I和无机试剂任选)。合成路线流程图例如下: 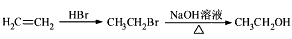
2014年雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
(1)CO2是大气中含量最高的一种温室气体,控制和治理CO2是解决温室效应的有效途径。目前,由CO2来合成二甲醚已取得了较大的进展,其化学反应是: 2CO2(g)+6H2(g)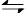 CH3OCH3(g)+3H2O(g) △H>0。
CH3OCH3(g)+3H2O(g) △H>0。
①写出该反应的平衡常数表达式。
②判断该反应在一定条件下,体积恒定的密闭容器中是否达到化学平衡状态的依据是。
| A.容器中密度不变 |
| B.单位时间内消耗2molCO2,同时消耗1mol二甲醚 |
| C.v(CO2)︰v(H2)=1︰3 |
| D.容器内压强保持不变 |
(2)汽车尾气净化的主要原理为:2NO(g)+2CO (g) 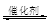 2CO2 (g) +N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断:
2CO2 (g) +N2 (g)在密闭容器中发生该反应时,c(CO2)随温度(T)、催化剂的表面积(S)和时间(t)的变化曲线,如图所示。据此判断: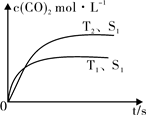
① 该反应的ΔH0(选填“>”、“<”)。
②当固体催化剂的质量一定时,增大其表面积可提高化学反应速率。若催化剂的表面积S1>S2,在右图中画出c(CO2)在T2、S2条件下达到平衡过程中的变化曲线。
(3)已知:CO(g)+2H2(g) CH3OH(g) rH =" -a" kJ•mol-1。
CH3OH(g) rH =" -a" kJ•mol-1。
①经测定不同温度下该反应的平衡常数如下:
| 温度(℃) |
250 |
300 |
350 |
| K |
2.041 |
0.270 |
0.012 |
若某时刻、250℃测得该反应的反应物与生成物的浓度为c(CO)="0.4" mol·L-1、c(H2)="0.4" mol·L-1、c(CH3OH)="0.8" mol·L-1,则此时v正v逆(填“>”、“<”或“=”)。
②某温度下,在体积固定的2L的密闭容器中将1 mol CO和2 mol H2混合,测得不同时刻的反应前后压强关系如下:
| 时间(min) |
5 |
10 |
15 |
20 |
25 |
30 |
| 压强比(P后/P前) |
0.98 |
0.90 |
0.80 |
0.70 |
0.70 |
0.70 |
达到平衡时CO的转化率为。
纳米级Cu2O由于具有优良的催化性能而受到关注,下表为制取Cu2O的三种方法:
(1)工业上常用方法Ⅱ和方法Ⅲ制取Cu2O而很少用方法Ⅰ,其原因是。
(2)已知:①2Cu(s)+1/2O2(g)=Cu2O(s)△H = -akJ·mol-1
②C(s)+1/2O2(g)=CO(g)△H = -bkJ·mol-1
③Cu(s)+1/2O2(g)=CuO(s)△H = -ckJ·mol-1
则方法Ⅰ发生的反应:2CuO(s)+C(s)= Cu2O(s)+CO(g)△H =kJ·mol-1。
(3)方法Ⅱ采用离子交换膜控制电解液中OH-的浓度而制备纳米Cu2O,装置如图所示,该电池的阳极反应式为。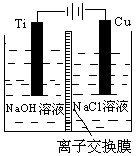
(4)方法Ⅲ为加热条件下用液态肼(N2H4)还原新制Cu(OH)2来制备纳米级Cu2O,同时放出N2。该制法的化学方程式为。已知肼与氨相似,则它与足量盐酸反应的方程式
(5)在相同的密闭容器中,用以上两种方法制得的Cu2O分别进行催化分解水的实验:
2H2O(g)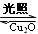 2H2(g)+ O2(g)△H>0 水蒸气的浓度随时间t变化如下表所示。
2H2(g)+ O2(g)△H>0 水蒸气的浓度随时间t变化如下表所示。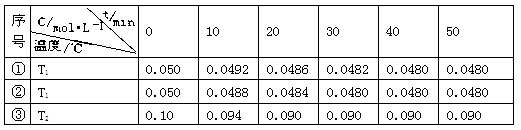
下列叙述正确的是(填字母代号)。
A.实验的温度:T2<T1
B.实验①前20 min的平均反应速率 v(O2)=7×10-5 mol·L-1 min-1
C.实验②比实验①所用的催化剂催化效率高