(9分)写出相对应的离子反应方程式或化学方程式:
①NaOH+NH4Cl==NaCl+NH3·H2O ___________________________________________
②(石灰乳)Ca(OH)2+H2SO4==CaSO4↓+2H2O_____________________________
③CO32-+2H+==CO2↑+H2O__________________________________________________;
甲醇是重要的化工原料,又可称为燃料。利用合成气(主要成分为CO、CO2和H2)在催化剂的作用下合成甲醇,发生的主反应如下:
①CO(g)+2H2(g) CH3OH(g);△H1
CH3OH(g);△H1
②CO2(g)+3H2(g) CH3OH(g)+H2O(g);△H2
CH3OH(g)+H2O(g);△H2
③CO2(g)+H2(g) CO(g)+H2O(g);△H3
CO(g)+H2O(g);△H3
回答下列问题:
(1)已知反应①中的相关的化学键键能数据如下:
| 化学键 |
H-H |
C-O |
CO的键能 |
H-O |
C-H |
| E/(kJ.mol-1) |
436 |
343 |
1076 |
465 |
413 |
由此计算△H1= kJ.mol-1,已知△H2=-58kJ.mol-1,则△H3= kJ.mol-1
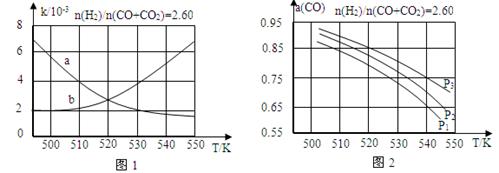
(2)反应①的化学平衡常数K的表达式为 ;图1中能正确反映平衡常数K随温度变化关系的曲线为 (填曲线标记字母),其判断理由是 。
|
在一个温度和体积不变的容器中,硫可以发生如下转化,其反应过程和能量关系如图1所示。(SO2(g)+1/2O2(g) SO3(g) ΔH=-98.45kJ·mol-1)
SO3(g) ΔH=-98.45kJ·mol-1)
(1)硫燃烧的热化学方程式为:__________________。
(2)恒容条件下,下列措施中能使n(SO2)/ n(SO3)比图1所示情况减小的有____________。
| A.降低温度 | B.充入He | C.再充入1 mol SO2(g)和1 mol O2(g) | D.使用催化剂 |
(3)恒温恒容时,图1中II到III反应放出的热量比1 mol SO2和2 mol O2充分反应放出的热量__________
(填 “多”、“少”或“相等”)。
(4)某SO2(g)和O2(g)体系,时间t1达到平衡后,改变某一外界条件,反应速率v与时间t的关系如图2所示,若不改变SO2(g)和O2(g)的量,则图中t2时引起平衡移动的条件可能是_____________;图中表示平衡混合物中SO3的含量最高的一段时间是_____________。(如t1~t2、t3~t4、t5~t6、t6~t7等)
用一种试剂除去下列各物质中的杂质(括号内的物质)。写出所用试剂及反应的离子方程式。
(1)BaCl2(HCl):试剂 ,离子方程式 。
(2)O2(CO2):试剂 ,离子方程式 。
(3)SO42-(CO32-):试剂 ,离子方程式 。
(4)Cu粉(Al粉):试剂 ,离子方程式 。
实验室用密度为1.84g·cm-3,溶质的质量分数为98%的硫酸,配制250mL物质的量浓度为0.46mol·L-1的硫酸。
(1)98%的浓硫酸的物质的量浓度为 。
(2)现有下列几种规格的仪器,应选用 (用序号填空)。
①10mL量筒 ②50 mL量筒 ③100mL量筒 ④100mL容量瓶 ⑤250mL容量瓶
(3)容量瓶上标有 、 和 。
(4)下列操作使所配溶液的物质的量浓度偏高的是 。
| A.往容量瓶中转移溶液时有少量液体溅出 | B.未洗涤稀释浓H2SO4的小烧杯 |
| C.定容时俯视刻度线 | D.洗净容量瓶未干燥即用来配制溶液 |
E.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
(1)8g CH4共有 mol氢原子,0.1molNH3共有约 个原子,同温同压下,同体积的NH3和H2S气体的质量比为 ;同温同压下,同质量的NH3和H2S气体的体积比为__ __。
(2)在标准状况下,15g某气体的分子数与11.2L CO的分子数相等,则该气体的摩尔质量为 。
(3)V L Fe2(SO4)3溶液中含Fe3+m g,则该溶液中Fe3+的物质的量浓度为_____ mol·L-1,溶质的物质的量浓度为______ mol·L-1。
(4)用脱脂棉包住约0.2g过氧化钠粉未,置于石棉网上,往脱脂棉上滴几滴水,可观察到脱脂棉燃烧起来。由实验现象所得出的有关过氧化钠和水反应的结论是:a:有氧气生成;b Na2O2和水反应的化学方程式是 。