室温下,CuSO4·5H2O(s)=Cu2+(aq)+SO42-(aq)+5H2O(l) ΔH1>0;
CuSO4(s)=Cu2+(aq)+SO42-(aq) ΔH2<0。
若CuSO4·5H2O受热分解的化学方程式为:CuSO4·5H2O(s)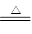 CuSO4(s) +5H2O(l),热效应为ΔH3。则下列判断正确的是
CuSO4(s) +5H2O(l),热效应为ΔH3。则下列判断正确的是
| A.ΔH1<ΔH3 | B.ΔH2>ΔH3 | C.ΔH1+ΔH3=ΔH2 | D.ΔH1+ΔH2=ΔH3 |
弱酸酸式盐的酸根离子电离和水解并存,已知HSO3—电离大于水解。以NaHXO3表示NaHCO3和NaHSO3。对于NaHCO3和NaHSO3溶液,下列关系式中不正确的是()
| A.c(Na+)+c(H+)=c(OH—)+c(HXO3—)+2c(XO32—) | B.c(Na+)= c(HXO3—)+ c(H2XO3)+c(XO32—) |
| C.c(Na+)> c(HXO3—)>c(H+)>c(OH—) | D.c(OH—)= c(H+)+ c(H2XO3)—c(XO32—) |
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中。下列关于这两种有机化合物的说法正确的是()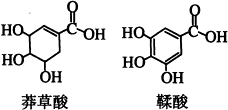
| A.鞣酸分子与莽草酸分子相比多了两个碳碳双键 |
| B.等物质的量的两种酸与足量金属钠反应产生氢气的量相同 |
| C.两种酸都能与溴水发生取代反应 |
| D.两种酸遇三氯化铁溶液都显色 |
下列离子方程式书写正确的是()
| A.NaHCO3溶液中加入过量的Ba(OH)2溶液: 2HCO3—+Ba2++2OH—====BaCO3â +2H2O+CO32— |
| B.FeCl3溶液与HI溶液反应:2Fe3++2HI=2Fe2++I2+2H+ |
| C.向AgCl悬浊液中滴加Na2S溶液,白色沉淀变成黑色: 2AgCl+S2—=Ag2S↓+2Cl— |
| D.石灰石与醋酸反应:CaCO3+2H+=Ca2++CO2↑+H2O |
下列关于“化学之最”,说法正确的是:()
①铝是地壳里含量最多的金属元素②油脂是产生能量最高的营养物质③H2O在第二周期和第VIA元素氢化物的沸点中均是最高的④乙炔是含碳量最高的烃⑤甲烷是含氢量最高的气态氢化物⑥HCl是卤化氢中沸点最低的⑦Na是短周期元素中原子半径最大的⑧Al3+是第三周期离子半径最小的
| A.①②④⑤⑦ | B.除④外全对 | C.①②⑤⑥ | D.全对 |
下列实验方法,正确的是()
| A.向试管中滴加液体,胶头滴管要紧贴试管内壁 |
| B.在实验室通过蒸馏的方法除去自来水中Cl— |
| C.将O2和H2的混合气体通过灼热的CuO除去其中的H2 |
| D.用核磁共振氢谱不能鉴别1—溴丙烷与2—溴丙烷 |