采用32%~35%的FeCl3溶液腐蚀印刷线路板上的金属铜,腐蚀废液中主要含有CuCl2、FeCl2和HCl等溶质。
(1)用FeCl3溶液溶解印刷线路板上金属铜的化学方程式为 。
(2)工业上用铁粉回收腐蚀废液中的铜,方法如下:
①用铁粉回收铜的操作为:加入过量铁粉,充分搅拌,过滤、洗涤、 。
②科学家对铁置换铜的工艺有如下研究:
分别在a、b、c三种条件下回收腐蚀废液中的铜,取充分反应后的粉末各3.000 g分别放入甲、乙、丙三个烧杯中,再加入100 mL 0.5mol·L-1的硫酸,水浴加热(70 ℃),搅拌,进行除铁处理。分别在第10、20、30、40、50 min时,用吸管移取0.5 g左右的铜试样于试管内,测定铜粉中铁的含量(质量分数),其结果如下图所示。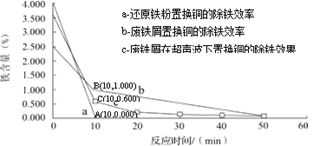
你认为除铁效果最好的是 (填“a”、“b”或“c”),其原因是 。
(3)工业上可用腐蚀废液制备CuCl2·2H2O,从而进行对废液的利用,其工艺流程如下: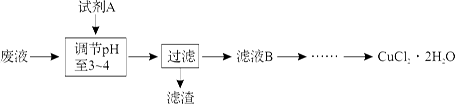
部分阳离子以氢氧化物形式沉淀时溶液的pH见下表:
| 沉淀物 |
Fe(OH)3 |
Fe(OH)2 |
Cu(OH)2 |
| 开始沉淀 |
2.3 |
7.5 |
4.7 |
| 完全沉淀 |
4.1 |
9.7 |
6.7 |
试剂A最好应选用 (填写字母代号),理由是 。
a.浓硫酸 b.Cl2 c.NaClO d.NaOH溶液
不粘锅之所以不粘,全在于锅底的那一层叫“特富龙”的涂料。特富龙是美国杜邦公司研发的含氟树脂的总称,包括聚四氟乙烯、聚全氟乙丙烯及各种含氟共聚物,PFOA(全氟辛酸铵)是生产特富龙过程中的必要添加剂。研究发现,特富龙在高温下,会释放出十几种有害气体,对健康有害。回答下列有关问题:
(1)聚四氟乙烯的合成途径如下所示:
写出由二氟一氯甲烷分解生成四氟乙烯(又称全氟乙烯)的反应方程式。
(2)聚全氟乙丙烯可看作是由四氟乙烯与全氟丙烯按物质的量比1:1通过反应(填反应类型)而得到,聚全氟乙丙烯的结构简式为。
(3)写出PFOA的化学式。
高纯氧化铝可用于制高压钠灯的陶瓷管,实验室制取高纯氧化铝的流程如下: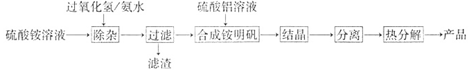
(1)“除杂”操作是加入过氧化氢后,用氨水调节溶液的pH约为8.0,以除去硫酸铵溶液中的少量Fe2+。检验Fe2+是否除尽的实验操作是。
(2)配制硫酸铝溶液时,需用硫酸酸化,酸化的目的是。
(3)上述流程图里,“结晶”这步操作中,母液经得到铵明矾(含结晶水)。
(4)上述流程图里,“分离”这个步骤应包含的是(填字母代号)
| A.蒸馏 | B.分液 | C.过滤 | D.洗涤晶体 |
2011年8月12日,《云南信息报》首度披露了云南曲靖铬污染事件,引起全国广泛关注。工业上将制取重铬酸钾(K2Cr2O7)和铬酸酐(CrO3)的剩余废渣称为铬渣,其成分为:SiO2、Al2O3、MgO、Fe2O3、CrO3、K2Cr2O7等。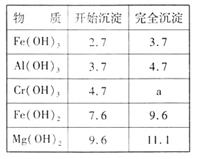
已知:①重铬酸钾和铬酸酐都易溶于水,这是造成铬污染的主要原因,它们都是强氧化剂,铬酸酐溶于水呈酸性;
②+6价铬易被人体吸收,可致癌:+3价铬不易被人体吸收,毒性小。
③右表为一些金属氢氧化物沉淀的pH参照数据。
回答下列处理铬渣、消除铬污染的有关问题:
(1)将铬渣用稀硫酸浸取、过滤,在浸出液中加入适量的绿矾(FeSO4·7H2O),加入绿矾的目的是。
(2)再向浸出液中缓慢加入烧碱,至pH刚好达到4.7,过滤,所得沉淀的化学式是;常温下,Cr(OH)3的溶度积Ksp=10-32,要使Cr3+完全沉淀[c(Cr3+)降至10-5mol·L-1视为沉淀完全],溶液的pH应调于a=。
(3)向(2)中得到的滤液中加入硫酸,调节至呈强酸性,所得的溶液是含溶质的溶液。
热重分析法是程序控制温度下,测量物质的质量与温度的关系的一种实验技术。现有一CaC2O4·nH2O试样,分别在氮气气氛、氧气气氛中进行热重分析,得到如下热重(TG)曲线。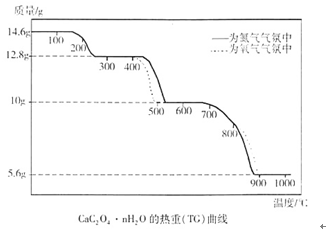
(1)图中曲线上有三个失重台阶,分别表示加热过程中依次发生了三个反应。根据第1步反应的失重数据计算试样CaC2O4·nH2O中的n值(精确到整数)为。
(2)根据第2步反应的失重数据推测第2反应的化学方程式为;观察曲线说明氧气存在时有利于第2步反应进行,原因是。
(3)第3步反应中释放的气体产物是。观察曲线可判断出,氧气存在时不利于第3步反应进行,可能原因是。
元素X、Y、Z、M、Q均为短周期主族元素,且原子序数依次增大。已知元素Y最高价氧化物对应水化物与它的氢化物反应能生成一种盐;Z原子最外层电子数与核外电子总数之比为3:4;M可与Z形成阴、阳离子个数比为1:2的两种化合物,Q原子的最外层电子数与次外电子数之比为3:4,YX3常温下为气体。
(1)化合物A、B由X、Z、M、Q四种元素中的三种组成的强电解质,且两种物质水溶液的酸碱性相同,组成元素的原子数目之比均为1:1:1,若A能抑制水的电离,B能促进水的电离,则化合物A的化学式为,B的化学式是。
(2)Se是人体必备的微量元素,与Q同一主族。该族二至五周期元素单质分别与H2反应生成1mol 气态氢化物的反应热如下,表示生成1 mol哂化氢反应热(△H)的是(填字母代号)。
A.+99.7kJ·mol-1B.+29.7 kJ·mol-1
C.-20.6 kJ·mol-1D.-241.8 kJ·mol-1
(3)X与Z、X与Q均可形成18电子分子甲和乙,写出甲、乙两种分子在水溶液中反应生成Q单质的化学方程式。X和Y也可形成18电子分子丙,它通常是一种液态火箭燃料。25℃、常压下,3.2g丙在氧气中完全燃烧放出热量为62.4kJ,请写出丙完全燃烧的热化学反应方程式。
(4)X、Y两种元素形成的离子化合物的电子式为。