设NA为阿伏伽德罗常数的值。下列叙述正确的是
| A.1mol羟基与17gNH3所含电子数都为NA |
| B.12.4g白磷(分子式为P4)中含有P—P共价键0.6NA |
| C.常温常压下,Na2O2与足量H2O反应,生成了0.2molO2,转移电子的数目为0.8 NA |
| D.适量铜粉溶解于1L0.5mol·L-1稀硝酸中,当生成2.24LNO时,溶液中氮原子数为0.4 NA |
已知X和Y能发生如下反应:X+Y===H2O+盐,下列有关物质X和Y所属类别的
判断中一定不正确的是
| A |
B |
C |
D |
|
| X |
酸 |
碱性氧化物 |
盐 |
羧酸 |
| Y |
碱 |
酸 |
碱 |
醇 |
下列电子式书写正确的是
A.溴化铵: |
B.硫化氢: |
C.氮气: |
D.羟基: |
向甲、乙、丙三个密闭容器中充入一定量的A和B,发生反应:xA(g)+B(g) 2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和下图表示:
2C(g)。各容器的反应温度、反应物起始量,反应过程中C的浓度随时间变化关系分别用下表和下图表示: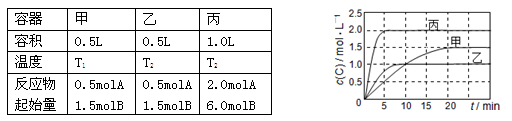
下列说法正确的是
A.T2时该反应的平衡常数K=0.8
B.由图可知:T1<T2,且该反应为吸热反应
C.前10min乙、丙两容器中v(A)乙>v(A)丙
D.C的质量m:m甲=m乙<2m丙
通过对实验现象的观察、分析推理得出正确的结论是化学学习的方法之一。对下列实验事实的解释正确的是
| 现象 |
解释 |
|
| A |
KI淀粉溶液中通入Cl2,溶液变蓝 |
Cl2能与淀粉发生显色反应 |
| B |
浓HNO3在光照条件下变黄 |
浓HNO3不稳定,生成有色产物NO2能溶于浓硝酸 |
| C |
某溶液中加入硝酸酸化的氯化钡溶液,有白色沉淀生成 |
说明该溶液中含有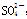 |
| D |
铜片放入浓硫酸中,无明显变化 |
说明铜在冷的浓硫酸中发生钝化 |
在一定温度条件下,甲、乙两个容积相等的恒容密闭容器中均发生如下反应:3A(g)+B(g) xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是
xC(g)+D(s),向甲中通入6molA和2molB,向乙中通入1.5molA、0.5molB和3molC和2molD,反应一段时间后都达到平衡,此时测得甲、乙两容器中C的体积分数都为0.2,下列叙述中正确的是
A、若平衡时,甲、乙两容器中A的物质的量相等,则x=4
B、平衡时,甲、乙两容器中A、B的物质的量之比不相等
C、平衡时甲中A的体积分数为40%
D、若平衡时两容器中的压强不相等,则两容器中压强之比为8∶5