(7分)实验室有一瓶试剂的标签破损不清如下图,
甲、乙、丙三位同学对它的主要成分进行讨论,一起猜想。
甲同学认为:该试剂主要成分是酸;
乙同学认为:该试剂主要成分是碱;
丙同学认为:该试剂主要成分是盐;
(1)你认为 同学的猜想是错误的;
(2)丙同学证实该物质是一种氮肥,则化学式是 ;
(3)甲同学对有关盐的知识进行了以下的整理。
| 氯化钾 |
氯化钙 |
氯化钠 |
氯化镁 |
氯化铝 |
氯化锌 |
氯化亚铁 |
氯化铜 |
| KCl |
CaCl2 |
NaCl |
MgCl2 |
AlCl3 |
ZnCl2 |
FeCl2 |
CuCl2 |
反思:
①根据以上盐中的金属元素的排列,可以得出是依据 顺序归纳整理的。
②酸在水溶液中能解离出H+,因此酸溶液具有相似的化学性质。据此分析上述盐溶液也会具有相似的化学性质,写出一种与上述盐溶液均能发生反应的物质的名称: 。
(4)小组同学探究:除去固体氯化钠中混有的氯化钙。
设计实验方案如下,请参与实验并回答问题。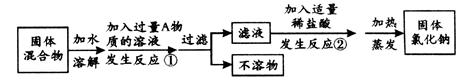
a.写出A物质的化学式: ;
b.反应②中如果加入的稀盐酸也过量,则对所得到的氯化钠纯度 (选填“有”或“没有”)影响;
c.分离后所得氯化钠的质量与分离前原混合物中氯化钠的质量相比较,结果 (选填“不变”、“增大”或“减小”)。
氢氧化钠溶液与稀硫酸发生中和反应时观察不到明显现象,为了确定其反应是否反生,某班同学设计了不同的实验方案进行探究:
(1) 方案一:向装有一定量氢氧化钠溶液的烧杯中滴几滴酚酞试液,不断滴入稀硫酸,如果实验现象是就可以证明氢氧化钠溶液与稀硫酸发生了化学反应;其反应的化学方程式为;
(2)方案二:向装有一定量稀硫酸的试管中滴加氢氧化钠溶液,振荡后再向其中滴加碳酸钠溶液,如果有气泡产生,则说明氢氧化钠溶液与稀硫酸没有发生化学反应。你认为方案二的结论正确吗?(填“正确”或“不正确”),理由是:
(3)下列实验方案中,能证明氢氧化钠溶液与稀硫酸发生了反应的是 (填序号)。
A.用pH试纸测定氢氧化钠溶液的pH,然后向其中滴加稀硫酸,pH逐渐减少,最终小于7
B.用温度计测试氢氧化钠溶液滴加稀硫酸前后的温度,温度明显上升
C.向一定量的氢氧化钠溶液中滴加稀硫酸后再滴加硫酸铜溶液,有蓝色沉淀生成
同学们在学习碱的化学性质时,进行了如图所示的实验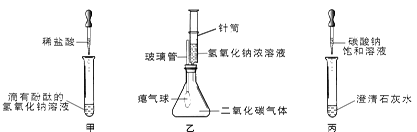
(1)写出甲实验中盐酸和氢氧化钠的反应。
(2)乙实验中滴加氢氧化钠溶液后,可观察到的现象是。
(3)丙实验中观察到试管内有白色沉淀产生。
(4)实验结束后,同学们将甲、乙、丙三个实验的废液倒入同一个干净的废液缸中,最终看到废液浑浊并呈红色。
1、提出问题:废液中含有哪些物质?
2、交流讨论:①一定含有的物质:碳酸钙、指示剂、水和(写物质名称)。
②还含有能使废液呈碱性的物质。能使废液呈碱性的物质是什么?同学们有
如下猜想。
小云认为:只有碳酸钠
小红认为:只有氢氧化钙
小林认为:是氢氧化钠和碳酸钠
3、实验设计:小方想用氯化钙溶液来验证小云、小红、小林的猜想。查阅资料获悉氯化钙、氯化钠溶液呈中性,并设计如下实验。请你将小方的实验设计补充完整。
| 实验内容 |
现象 |
结论 |
| 取少量废液缸中上层清液于试管中,加入过量氯化钙溶液,静置。 |
①有白色沉淀,溶液呈红色。 |
的猜想正确。 |
| ②。 |
小云的猜想正确。 |
|
| ③。 |
的猜想正确。 |
4、反思拓展:在分析化学反应后所得物质的成分时,除了考虑生成物外还需考虑
通过1个多月的化学学习,应该知道有多种途径可以制取氧气。请根据下列装置,回答问题:
⑴写出标号①②的仪器名称:①,②。
⑵实验室要收集较纯净O2,可选用装置是(填写装置序号);
⑶用排水法收集氧气,当气泡时,再开始收集;
⑷用高锰酸钾制取O2的文字表达式为,若实验结束发现水槽中的水变成了浅紫红色,你认为产生该现象的原因可能是;若实验结束后发现大试管有裂痕,可能的原因是(写一点)。
若用高锰酸钾制取氧气的操作步骤分为:a给试管加热 b导管移出水面
c检查装置的气密性d排水法收集氧气e熄灭酒精灯 f将反应物加入试管
用带有导管的橡皮塞塞紧并把它固定在铁架台上;其操作的正确顺序是: ___________。
⑸若分解过氧化氢制取氧气,写出反应的文字表达式可选用的发生装置是(填写装置序号)。
化学课外活动中,小红将稀盐酸加入盛有澄清石灰水的试管中,无明显现象;小强将稀盐酸加入盛有K2CO3溶液的试管中,有气体生成.反应结束后,两同学把废液倒入同一废液缸中,观察到废液缸中产生少量的气泡,最终有白色沉淀生成.请回答以下问题:
(1)废液缸中最终生成的白色沉淀是。
(2)通过分析废液缸中的现象,你认为小红实验后的废液中一定含有的溶质是。
(3)小强从废液缸中取出废液,过滤,对滤液进行实验探究.他认为滤液中除含有KCl外,还可能含有K2CO3,请你邦他完成下面的实验报告:
| 实验操作 |
实验现象 |
实验结论 |
| 取少量滤液于试管中,加入 |
废液中含K2CO3 |
小明发现家中一枚戒指生满了铜绿,他和同学利用这枚戒指展开了研究性学习。
《查阅资料》 真金在空气中不会生锈,生满铜绿的"金戒指"材质为铜锌合金;
铜长期露置在潮湿的空气中能生成铜绿,其主要成分是碱式碳酸铜,碱式碳酸铜受热易分解生成
和
。
据上述资料可推知,碱式碳酸铜由种元素组成。
《 实验探究》 将该枚戒指加入过量稀盐酸中,有气泡产生,溶液由无色逐渐变为蓝绿色。
(1)小明认为:气体中除了含有
,还可能含有少量。
(2)小红认为蓝绿色溶液中的溶质只有氯化锌。小华认为溶液中的溶质除了氯化锌外,
还应该含有、。他取适量上述蓝绿色溶液,加入光亮的铁片,观察到了现象:①,②,证实了自己的观点。
(3)小娟取适量新制的
溶液,加入锌粒,一段时间后,溶液颜色变浅。结合小华的实验可推知:铁、锌、铜三种金属的活动性由弱到强的顺序是。
(4)小明想进一步探究"金戒指"中铜元素的含量,取一枚同材质的"金戒指",称得质量为
。在老师的指导下,将"金戒指"经浓硝酸氧化、碱化等步骤处理后,最终得到纯净的氧化铜,称得质量仍然为
(实验过程中铜元素损失忽略不计)。则"金戒指"中铜元素的质量分数是多少?(写出计算过程)