两种气态烃的混和物共0.1mol,完全燃烧后得3.36L(标况下)CO2和3.6g水,下列说法正确的是
| A.一定有乙烯 | B.可能有甲烷 |
| C.可能有乙烷 | D.一定是甲烷和乙烯的混和物 |
下列叙述正确的是
| A.Cu2O是一种半导体材料,基于绿色化学理念设计的制取Cu2O的电解池示意图如图一所示,石墨电极上产生氢气,铜电极发生氧化反应 |
| B.图一所示当有0.1mol电子转移时,有0.1molCu2O生成 |
| C.图二装置中发生:Cu+2Fe3+ = Cu2++2Fe2+,X极是负极,Y极材料可以是铜 |
| D.如图二,盐桥的作用是传递电荷以维持电荷平衡,Fe3+经过盐桥进入左侧烧杯中 |
【原创】下列说法不正确的是
| A.用新制氢氧化铜悬浊液可以鉴别乙酸、葡萄糖和淀粉三种溶液 |
| B.分子式为C6H12的某链状有机物,若6个碳原子在同一平面上,则与氢气加成后产物的名称为2,3-二甲基丁烷 |
C.已知某反应方程式为 ,生成物中带“※”号的C原子来自“ ,生成物中带“※”号的C原子来自“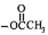 ”中的甲基 ”中的甲基 |
| D.硬脂酸甘油酯和油酸甘油酯互为同系物 |
【改编】X、Y、Z、W为短周期元素,原子半径X>Y>Z>W,X、Y、Z处于同一周期,Z、W处于同一主族,X、Y、Z原子序数之和为40,X是短周期中除稀有气体元素外半径最大的元素。下列说法正确的是
| A.若X、Y、W形成的化合物为XYW2,则其水溶液可以显碱性 |
| B.Y的最高价氧化物对应的水化物一定是碱 |
| C.稳定性:W的氢化物>Z的氢化物,沸点:Z的氢化物>W的氢化物 |
| D.X、Y的氧化物晶体类型一定相同 |
下列有关实验操作说法正确的是
| A.吸液时左手拿洗耳球右手持移液管;放液时应将移液管倾斜放入垂直放置的容器中 |
| B.用碱式滴定管量取23.10 mL 0.20 mol·L-1高锰酸钾溶液 |
| C.用10 mL量筒量取5.2 mL稀硫酸,仰视时实际量得的液体体积大于5.2 mL |
| D.钠、钾、白磷均应保存在煤油中,取用它们时要用镊子夹取 |
下列说法正确的是
| A.科学家在研究物质微观结构的过程中先后使用了光学显微镜、电子显微镜、扫描隧道显微镜等观测仪器 |
| B.H2O2在过氧化氢酶的催化下,随着温度的升高,分解速率持续加快 |
| C.甲醇、肼、氨等燃料电池的能量转换效率远高于普通燃料燃烧的能量转化效率 |
| D.钠和钾的合金在室温下呈液态,可用于快中子反应堆作热交换剂 |