下列有关实验的说法中错误的是:
| A.在蒸馏的实验中,温度计的水银球位于支管口处是为了测出馏分的沸点; |
| B.用直接蒸馏的方法不能得到无水乙醇; |
| C.在重结晶的实验中,使用短颈漏斗趁热过滤是为了减少被提纯物质的损失; |
| D.作为重结晶实验的溶剂,杂质在此溶剂中的溶解度受温度影响应该很大。 |
一定条件下,可逆反应X(g)+3Y(g) 2Z(g);若X、Y、Z起始浓度分别为C1、C2、C3(均不为0),平衡时X、Y、Z的浓度分别为0.1mol/L、0.3 mol/L、0.08 mol/L,则下列判断不合理的是
2Z(g);若X、Y、Z起始浓度分别为C1、C2、C3(均不为0),平衡时X、Y、Z的浓度分别为0.1mol/L、0.3 mol/L、0.08 mol/L,则下列判断不合理的是 
| A.C1:C2=1:3 | B.平衡时,Y和Z的生成速率之比为3 :2 |
| C.反应过程中X、Y的转化率不相等 | D.C1取值范围为0<C1<0.14 mol/L |
常温下,甲溶液中水电离出的H+浓度为10-12 mol/L,乙溶液中水电离出的H+浓度为
10-2mol/L,下列说法正确的是
| A.甲、乙两溶液的pH不可能相同 |
| B.甲、乙两种溶液中加入Al粉都一定会产生H2 |
| C.HCO3-不可能在甲、乙两溶液中大量共存 |
| D.甲不可能是盐溶液,乙不可能是酸或碱溶液 |
对化学平衡移动的分析,下列说法不正确的是
①已达平衡的反应C(s)+H2O(g) CO(g)+H2(g),当增加反应物的物质的量时,平衡一定向正反应方向移动
CO(g)+H2(g),当增加反应物的物质的量时,平衡一定向正反应方向移动
②已达平衡的反应N2(g)+3H2(g) 2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
2NH3(g),当增大N2的浓度时,平衡向正反应方向移动,N2的转化率一定升高
③改变外界条件使正反应速率大于逆反应速率时,化学平衡向正反应方向移动
④有气体参加的反应达平衡时,在恒压反应器中充入稀有气体,平衡不一定移动
| A.①④ | B.①③ | C.②③ | D.①② |
下列各装置中都盛有0.1 mol·L—1的NaCl溶液,放置相同时间后,锌片的腐蚀速率由快到慢的顺序是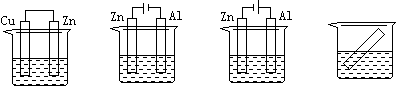
① ② ③ ④
| A.③①④② | B.①②④③ | C.②①④③ | D.②①③④ |
下列离子方程式书写正确的是
A.NaHS水解反应:HS-+ H2O  H3O++ S2- H3O++ S2- |
B.明矾加入在水中起净化作用的原因:Al3++ 3H2O  Al(OH)3(胶体) + 3H+ Al(OH)3(胶体) + 3H+ |
C.氢氧化钡溶液与稀硫酸反应: |
| D.碳酸氢钠溶液中加入过量Ba(OH)2溶液: |
2HCO3- + Ba2+ + 2OH- = BaCO3↓+ CO32-+ 2H2O