设NA表示阿伏加德常数的数值,下列叙述中不正确的是
| A.常温常压下,20g D2O和足量的金属钠反应产生气体的分子数为0.5NA |
| B.常温常压下,32g O2—离子中所含电子的数目为17NA |
| C.含0.01mol H2O2的水溶液跟MnO2充分作用,反应过程中转移的电子总数0.02NA |
| D.53g Na2CO3固体含有的离子数为1.5NA |
体积相同的甲、乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2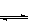 2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )
2SO3,并达到平衡。在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率( )
| A.等于p% | B.大于p% | C.小于p% | D.无法判断 |
某温度下的定容密闭容器中,进行可逆反应:A(s)+2B(g) C(g)+D(g),当下列物理量不发生变化时:①混合气体的密度;②容器内气体的压强;③混合气体的平均相对分子质量;④B的物质的量浓度。则能表明该反应一定已达到平衡状态的是()
C(g)+D(g),当下列物理量不发生变化时:①混合气体的密度;②容器内气体的压强;③混合气体的平均相对分子质量;④B的物质的量浓度。则能表明该反应一定已达到平衡状态的是()
| A.只有④ | B.②③ | C.②③④ | D.①③④ |
对于反应:N2+O2 2NO,在密闭容器中进行,下列条件能加快反应速率的是()
2NO,在密闭容器中进行,下列条件能加快反应速率的是()
| A.缩小体积使压强增大 |
| B.降低体系温度 |
| C.体积不变充入He使气体压强增大 |
| D.保持总压强不变,充入Ne气体 |
已知450℃时,反应H2(g)+I2(g)  2HI(g)的K=50,由此推测在450℃时,反应
2HI(g)的K=50,由此推测在450℃时,反应
2HI(g)  H2(g)+I2(g)的化学平衡常数为( )
H2(g)+I2(g)的化学平衡常数为( )
| A.50 | B.0.02 | C.100 | D.无法确定 |
甲烷是一种高效清洁的新能源,0.25mol甲烷完全燃烧生成液态水时放出222.5KJ热量,则下列热化学方程式中正确的是( )
| A.2CH4(g) + 4O2(g) ==2CO2(g) + 4H2O(l);ΔH==+890KJ·mol—1 |
| B.CH4(g) + 2O2(g) ==CO2(g) +2H2O(l);ΔH==+890KJ·mol—1 |
| C.CH4(g) + 2O2(g) ==CO2(g) +2H2O(l);ΔH==-890KJ·mol—1 |
| D.2CH4(g) + 4O2(g) ==2CO2(g) + 4H2O(l);ΔH==-890KJ·mol—1 |